|
|
Citocromo bc1 |
|||||
|
Molecola del Mese di Maggio 2011 Nella catena respiratoria il citocromo bc1 è il complesso 3, una pompa protonica azionata da un flusso di elettroni 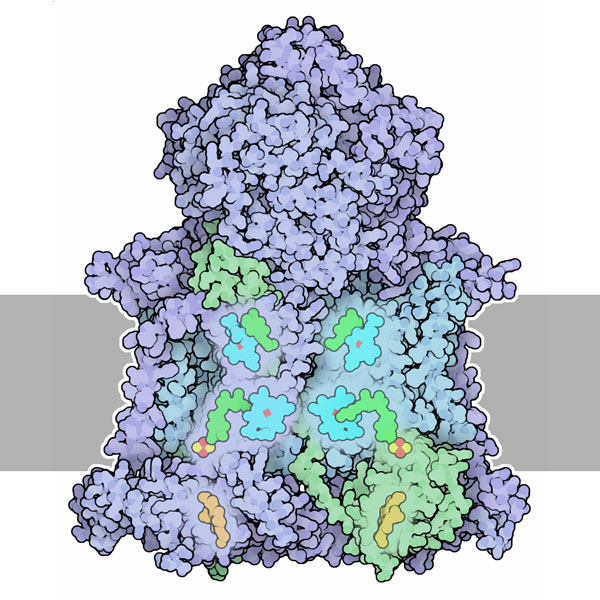 Introduzione IntroduzioneLe cellule sono bravissime nel ricavare fino all'ultima goccia di eneregia dal cibo. Con il glucosio, realizzano una serie di reazioni che lo trasformano in acqua e CO2 come in una normale combustione. Naturalmente nelle cellule non si sprigionano fiamme, ma avvengono delle reazioni controllate a bassa temperatura. L'ossidazione delle molecole di glucosio avviene ad opera del NAD+ che viene ridotto a NADH. Le cellule ricavano, alla fine, grandi quantità di energia dal processo quando il NADH viene riossidato a NAD+ nei mitocondri per opera dell'ossigeno O2. Gli elettroni però non passano direttamente dal NADH all'O2, ma devono attraversare la catena respiratoria, una serie di complessi proteici che contengono delle pompe protoniche che, al passaggio degli elettroni, trasferiscono ioni H+ da un lato all'altro della membrana. Questi protoni, accumulati fuori dalla membrana interna dei mitocondri, mettono in rotazione l'enzima ATP sintasi (mdm 12-2005) quando tornano verso la parte più interna dei mitocondri, verso la loro posizione iniziale. Pompare protoni Il citocromo bc1 mostrato qui sopra (chiamato anche complesso 3, file PDB 3h1j) è la pompa protonica centrale in questo processo. Si lega all'ubichinolo (QH2 verde), un trasportatore di elettroni e protoni che si trova nella membrana dei mitocondri (proveniente dal complesso 1, mdm 12-2011) e  prende
da questo due elettroni e due protoni. I due protoni vengono rilasciati
sul lato esterno della membrana dove mettono in azione l'ATP sintasi.
I due elettroni invece seguono due strade diverse. prende
da questo due elettroni e due protoni. I due protoni vengono rilasciati
sul lato esterno della membrana dove mettono in azione l'ATP sintasi.
I due elettroni invece seguono due strade diverse. Un elettrone si dirige con forza verso il centro ferro-zolfo (giallo e rosso) e da qui giunge all'eme c1 (giallo) che si trova sul lato esterno della membrana. L'altro elettone fa un percorso meno favorevole che lo porta all'eme bH e poi all'eme bL (entrambi azzurri) vicino al lato interno della membrana. Qui si lega ad una molecola di ubichinone (Q) che ha già perso i suoi due idrogeni e così gli consente di legarsi ad un nuovo H+ proveniente dal lato interno della membrana formando una molecola intermedia (chinidrone QH.) che poi può sommare un altro elettrone e un altro H+ per formare ubichinolo QH2, questo si presenta nella parte esterna della membrana per ricominciare il processo (vedi anche lo schema qui a fianco). Il processo che avviene nel percorso meno favorevole forma quindi un ciclo, chiamato ciclo Q. Questo fa sì che ogni elettrone che fluisce nel citocromo bc1 sposti 2 protoni dal lato interno a quello esterno della membrana: un protone con il primo ubichinolo, l'altro con il secondo ubichinolo formato nel ciclo Q, grazie alla forza con la quale gli elettroni fluiscono verso l'eme c1 e il citocromo c (mdm 12-2002) nel primo percorso. Cofattori complessi Il citocromo bc1 è un complesso proteico dimero. Ognuna delle due parti è composta da 11 catene proteiche e da più cofattori, tre gruppi eme: bH, bL, c1, e un centro ferro-zolfo. Sono state ottenute le strutture di molti tipi di citocromo bc1, quella mostrata qui sopra è di mitocondrio di pollo (PDB file 3h1j). Questa struttura ha permesso di individuare l'esatta posizione dei cofattori e il percorso seguito dagli elettroni, ma ha permesso anche di scoprire altri dettagli sul funzionamento del citocromo bc1 come lo strano movimento della proteina che contiene il centro ferro-zolfo. Gli scienziati stanno ancora cercando di capire come il flusso di elettroni possa avvenire senza che il ciclo vada in corto circuito.  Fotosintesi Anche nel processo della fotosintesi, che avviene nelle cellule vegetali, è presente una pompa protonica spinta da un flusso di elettroni. Anche qui si crea un accumulo di protoni su un lato della membrana che mette in moto l'enzima ATP sintasi. Qui però il flusso di elettroni è rovescio rispetto a quello dei nostri mitocondri grazie all'energia della luce che eccita a tal punto l'elettrone iniziale da consentirgli di fare il percorso in senso opposto a quello che percorrerebbe spontaneamente. Nella fotosintesi, infatti, gli elettroni vengono prelevati dall'ossigeno dell'acqua (che così diventa O2) e portati al NADH. Nella prima fase di questo processo, due elettroni giungono ad un trasportatore simile all'ubichinone, il plastochinone PQH2 che lega anche due protoni. Questo trasporta il suo carico fino al citocromo b6f, mostrato qui a destra dal file PDB 1vf5, che usa questi atomi di idrogeno in un ciclo simile al ciclo Q per spostare protoni attraverso la membrana del cloroplasto. La destinazione finale di questi elettroni è la plastocianina invece del citocromo c. Esplorando la struttura 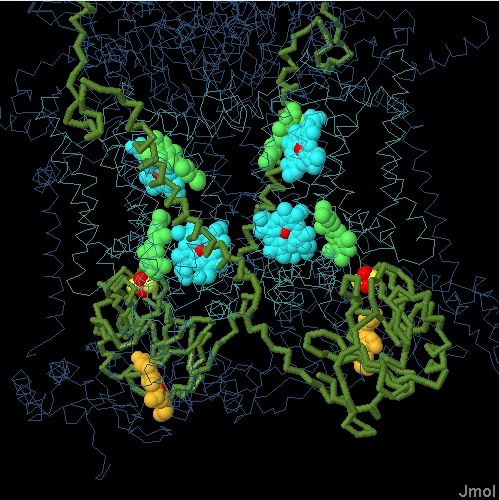 La
struttura del citocromo bc1 ha rivelato il percorso fatto dagli elettroni
e i siti di legame per l'ubichinolo, ma ha mostrato anche un
fatto del tutto inatteso. Il percorso degli elettroni verso il citocromo
c passa attraverso un centro ferro-zolfo e
un gruppo eme c1 che poi cede gli elettroni al citocromo c. Queste strutture
hanno dimostrato che la catena proteica che contiene il centro ferro-zolfo
non resta ferma, ma può spostarsi, prima portandosi
a ridosso dell'ubichinolo dove si carica con un elettrone, e poi
spontandosi in basso verso il gruppo eme c1 (arancione), a
cui cede l'elettrone. La
struttura del citocromo bc1 ha rivelato il percorso fatto dagli elettroni
e i siti di legame per l'ubichinolo, ma ha mostrato anche un
fatto del tutto inatteso. Il percorso degli elettroni verso il citocromo
c passa attraverso un centro ferro-zolfo e
un gruppo eme c1 che poi cede gli elettroni al citocromo c. Queste strutture
hanno dimostrato che la catena proteica che contiene il centro ferro-zolfo
non resta ferma, ma può spostarsi, prima portandosi
a ridosso dell'ubichinolo dove si carica con un elettrone, e poi
spontandosi in basso verso il gruppo eme c1 (arancione), a
cui cede l'elettrone. Nella figura qui a fianco (file PDB 1ntz) si può vedere la struttura dimera del citocromo bc1. Osservandone la metà di sinistra dall'alto verso il basso, si notano nell'ordine: due gruppi eme bL e bH (azzurri), che rappresentano i due siti di legame per le due molecole di ubichinolo (verde chiaro) nelle due fasi del ciclo Q. Più in basso si nota il centro ferro-zolfo (giallo e rosso) legato alla catena proteica (verde oliva) capace di muoversi e che qui ha portato in sù il centro ferro-zolfo vicino all'ubichinolo. Più sotto si vede il gruppo eme c1 (arancione) isolato. In alto l'eme bL cede un elettrone all'ubichinone (vedi anche lo schema mostrato sopra) In mezzo l'ubichinolo cede un elettrone all'eme bH (che lo manda in alto all'eme bL) e cede un secondo elettrone al centro ferro- zolfo. 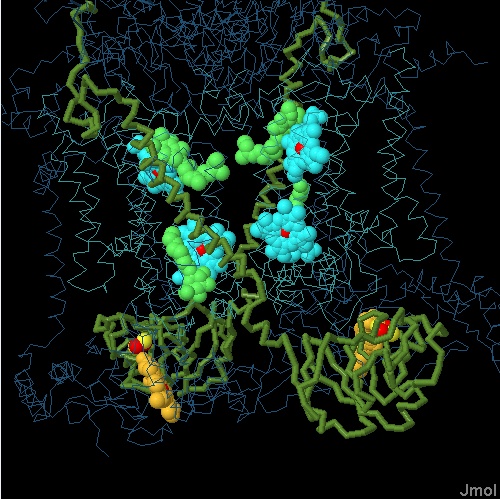 In
basso il centro ferro-zolfo è troppo lontano dal gruppo
eme c1 In
basso il centro ferro-zolfo è troppo lontano dal gruppo
eme c1 per potergli cedere l'elettrone appena ricevuto. Nella figura qui a fianco (file PDB 1bcc, citocromo bc1 di pollo) si può apprezzare il grande movimento compiuto dalla proteina (verde oliva) che regge il centro ferro-zolfo. Questa ha cambiato conformazione dopo che il centro ferro-zolfo ha ricevuto l'elettrone dall'ubichinolo. Ora il centro ferro-zolfo si trova vicino all'eme c1 e gli può cedere l'elettrone che da qui giungerà al citocromo c come si vede nella prossima figura. 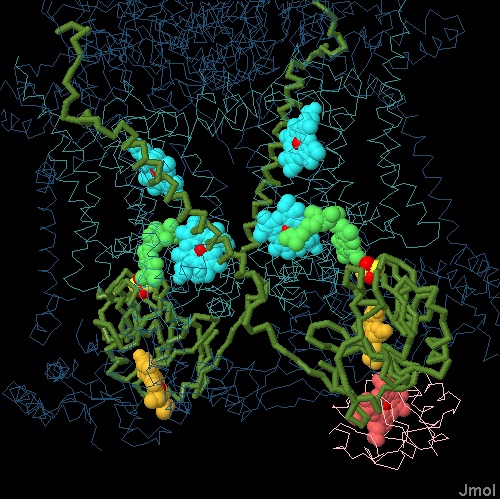 In quest'ultima figura (file PDB 1kyo, citocromo bc1 di lievito) si vede il citocromo c col suo eme c (rosso, in basso a destra) che si è legato a ridosso dell'eme c1 dal quale preleva l'elettrone. Successivamente il citocromo c, muovendosi esternamente alla membrana, può portare l'elettrone al prossimo complesso proteico della catena respiratoria, il complesso 4. Spunti per ulteriori esplorazioni 1. Sono stati scoperti molti farmaci che si legano ai siti dell'ubichinolo nel citocromo bc1. Cercate questi farmaci negli archivi PDB e valutate la loro somiglianza con la molecola dell'ubichinolo. 2. Il citocromo b6f usa un meccanismo simile a quello del citocromo bc1 per accoppiare il trasporto di elettroni al trasporto di protoni. Confrontate i due complessi e notate che il citocromo b6f ha alcuni cofattori extra. Gli scienziati non hanno ancora stabilito quale sia il ruolo di questi cofattori, provate anche voi a fare delle ipotesi. A. R. Crofts (2004) The cytochrome bc1 complex: function in the context of structures. Annual Review of Physiology 66, 689-733. J. L. Cape, M. K. Bowman and D. M. Kramer (2006) Understanding the cytochrome bc complexes by what they don't do. The Q-cycle at 30. Trends in Plant Science 11, 46-55. D. Baniulis, E. Yamashita, H. Zhang, S. S. Hasan and W. A. Cramer (2008) Structure-function of the cytochrome b6f complex. Photochemistry and Photobiology 84, 1349-1358.
|
||||||
|
|
||||||
