|
|
Citocromo c |
|||||
|
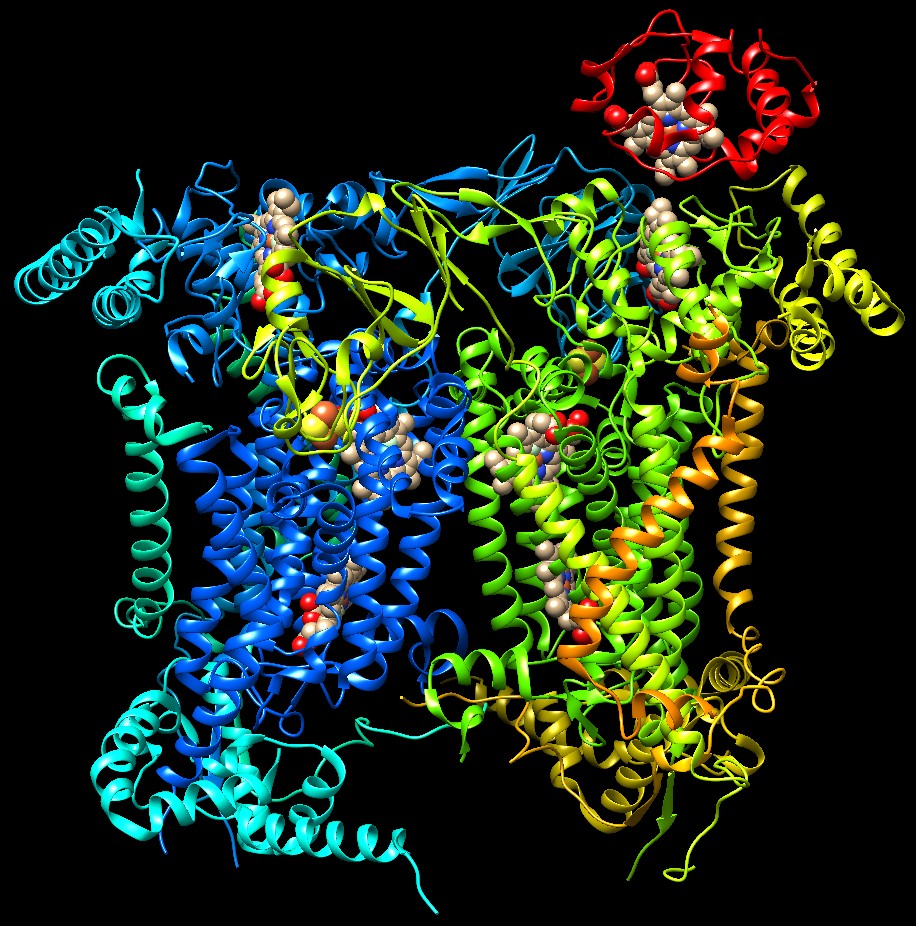
Molecola del mese di dicembre 2002 Il citocromo c trasporta elettroni dal complesso 3 al complesso 4 della catena di trasporto degli elettroni 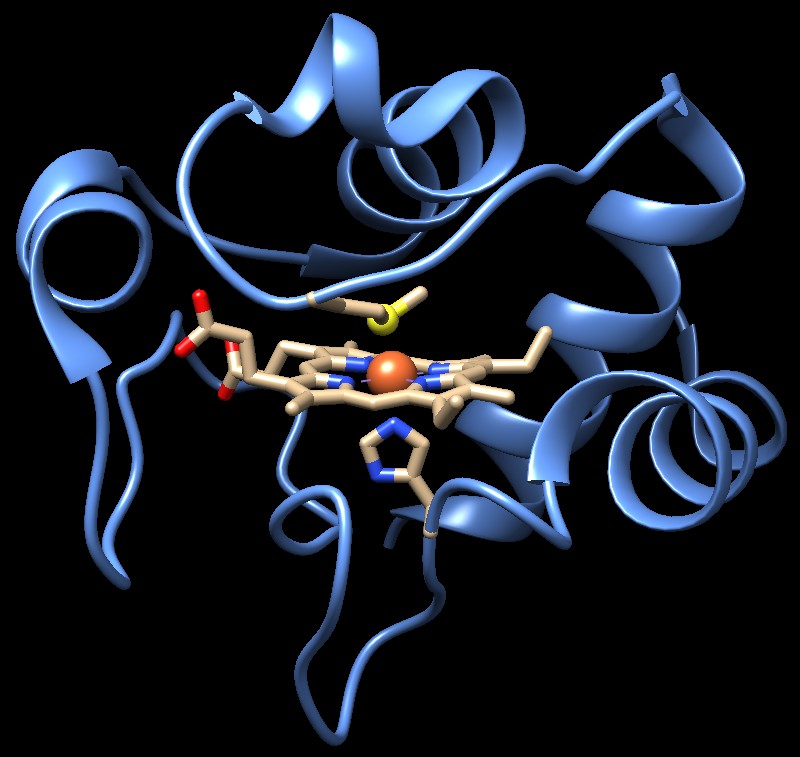 Introduzione IntroduzioneL'elettricità è un fenomeno comune nel nostro mondo, fa funzionare quasi tutto: dalle luci nella nostra stanza, al computer di fronte a noi. L'elettricità è costituita da un flusso di elettroni all'interno di un materiale conduttore, come per esempio un filo di rame. Gli elettroni fluiscono scorrendo nello spazio tra gli atomi lungo il filo. Anche le cellule usano l'elettricità per dare energia a molti processi, ma qui gli elettroni si muovono in un modo molto diverso. Non fluiscono in modo continuo lungo un filo sottile all'interno della cellula, ma vengono trasportati uno alla volta, saltando da una proteina all'altra attraverso una serie di reazioni chimiche. Quando l'elettrone arriva si hanno reazioni di riduzione, quando l'elettrone se ne va si hanno reazioni di ossidazione. In questo modo, gli elettroni vengono presi da una particolare molecola e portati esattamente dove sono necessari. Trasportare elettroni Il citocromo c, mostrato qui sopra (file PDB 3cyt), è un trasportatore di elettroni. Come molte proteine che trasportano elettroni, contiene un coenzima speciale in grado di maneggiare elettroni ossidandosi e riducendosi. Il citocromo c contiene un gruppo eme che ha uno ione ferro (arancione) saldamente legato al centro. Il gruppo eme è tenuto in posizione da una istidina (sotto) e da una metionina (sopra) che si lega al ferro col suo atomo di zolfo (giallo). Lo ione ferro è in grado di accettare o rilasciare un elettrone passando dallo stato di Fe3+ a Fe2+ e viceversa. La proteina circostante crea l'ambiente ideale per l'elettrone, regolando con precisione la forza (il potenziale V) con cui viene trattenuto. Una famiglia prestigiosa Il citocromo c è una proteina antica che si è formata molto presto nel corso dell'evoluzione. Dato che questa proteina svolge un ruolo essenziale nella produzione di energia nella cellula, ha subito pochi cambiamenti nel corso dei milioni di anni. Quindi si possono trovare forme molto simili di citocromo c nelle cellule di lievito, in quelle vegetali o nelle nostre cellule. Negli archivi PDB, comunque, c'è una vasta raccolta di altre molecole trasportatrici di elettroni. Vi sono molti tipi di citocromo, tutti usano il ferro eme per trasportare elettroni, ma cambia la proteina che circonda il gruppo eme e questo li mette in grado di lavorare a potenziali diversi. Altri trasportatori usano coenzimi diversi per trasportare elettroni, come i gruppi ferro-zolfo (ferredossina), gli ioni rame dal caratteristico colore blu chiaro (azurina e plastocianina) o gli ioni di metalli più esotici. Come il citocromo c, ognuna di queste proteine rappresenta una singola connessione nel circuito elettrico cellulare, trasportando elettroni da un punto ad un altro della catena di trasporto degli elettroni. 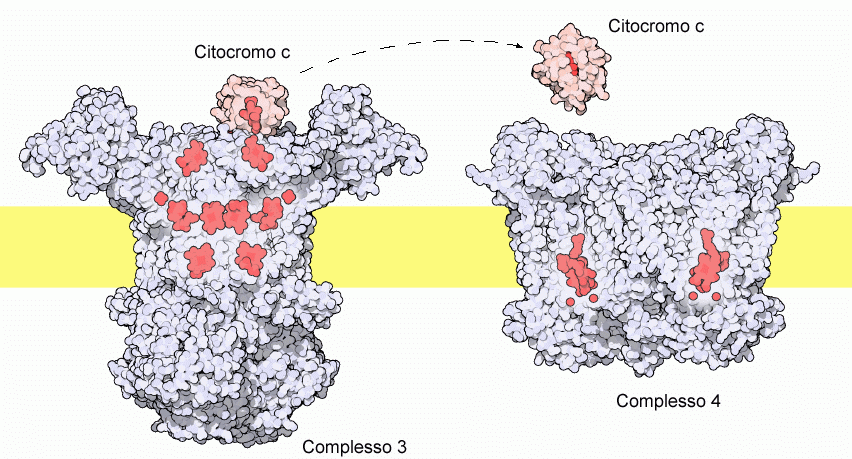 Circuiti cellulari Il citocromo c costituisce una delle tante connessioni in una specie di circuito elettrico cellulare, la catena di trasporto degli elettroni, che rappresenta l'ultimo passaggio nella produzione di energia nella cellula (respirazione cellulare). Gli elettroni provenienti dalla degradazione dello zucchero (glucosio), alla fine giungono all'ossigeno che viene trasformato in acqua (il destino finale dell'ossigeno che respiriamo). Il citocromo c, la piccola proteina rosa nella figura qui sopra, trasferisce singoli elettroni tra il compless 3 e il complesso 4 della catena. Raccoglie gli elettroni dal complesso 3 (mdm 5/2011) che contiene i citocromi b e c1 (file PDB 1kyo) e li consegna al complesso 4 chiamato citocromo c ossidasi (mdm 5/2000) che contiene i citocromi a e a3 (file PDB 1oco). I complessi 1, 3 e 4 si comportano come delle macchine elettriche, infatti usano l'energia degli elettroni che scorrono al loro interno per compiere del lavoro. Mentre gli elettroni fluiscono attraverso i loro gruppi trasportatori (mostrati in rosso nella figura qui sopra) pompano ioni H+ dal lato inferiore a quello superiore della membrana interna dei mitocondri in cui sono immersi (striscia gialla). Questi ioni H+ sono poi usati per dare energia alla produzione di ATP. Il citocromo c fa in modo che questa macchina così complessa funzioni correttamente, trasportando elettroni dal complesso 3 al complesso 4 muovendosi nella soluzione fuori dalla membrana interna. Esplorando la struttura
|
||||||
|
|
||||||