|
|
Lattato deidrogenasi |
|||||
|
Molecola del Mese di Giugno 2008 Le nostre cellule, durante uno sforzo muscolare intenso, producono acido lattico se l'apporto di ossigeno è insufficiente  Introduzione IntroduzioneL'enzima lattato deidrogenasi è una valvola di sicurezza nella nostra linea di produzione di energia. Per la maggior parte del tempo le nostre cellule degradano completamente il glucosio trasformandolo in anidride carbonica (CO2), e acqua (H2O). Questo processo di ossidazione, però, richiede molto ossigeno, quindi, quando il suo apporto è insufficiente, la linea di produzione dell'energia deve essere fermata alla fine della glicolisi (mdm febbraio 2004). L'enzima lattato deidrogenasi è la via con la quale le cellule risolvono, almeno temporaneamente, questo problema. Ginnastica aerobica Quando facciamo un esercizio fisico aerobico il nostro respiro si fa più frequente, il cuore batte più velocemente e alle nostre cellule arriva una grande quantità di ossigeno. Questo viene utilizzato come ossidante per trasformare il glucosio in acqua e CO2 con una sequenza di reazioni che è chiamata respirazione cellulare che serve a produrre energia sotto forma di ATP. . . . . . 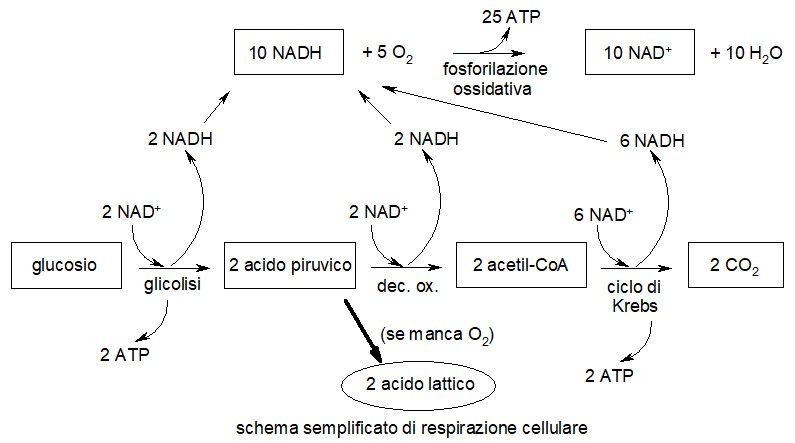
Quando, però, l'esercizio fisico è molto intenso, come nella corsa veloce, le cellule non hanno abbastanza ossigeno per produrre tutta l'energia che serve. In questo caso usano la glicolisi come fonte primaria di energia. Anche la glicolisi, però, è un processo ossidativo, in uno dei suoi passaggi uno ione idrogeno negativo H- è trasferito dal glucosio al NAD+ per formare NADH. Normalmente questi atomi di idrogeno sono poi trasferiti all'ossigeno per formare acqua. Se, però, l'ossigeno non è disponibile, il NADH si accumula e quindi non c'è abbastanza NAD+ per continuare la glicolisi e produrre ATP. A questo punto entra in azione l'enzima lattato deidrogenasi (LDH) che consente di ossidare il NADH a NAD+ utilizzando come molecola ossidante, al posto dell'ossigeno, il prodotto stesso della glicolisi, l'acido piruvico, che viene ridotto ad acido lattico secondo la reazione: . . . . . . . . . . . . . . . . . . . . 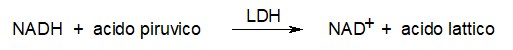 Il NAD+ diventa così ancora disponibile e può essere riutilizzato per continuare a svolgere la glicolisi e produrre energia. . . . . . . . . . . . . . . 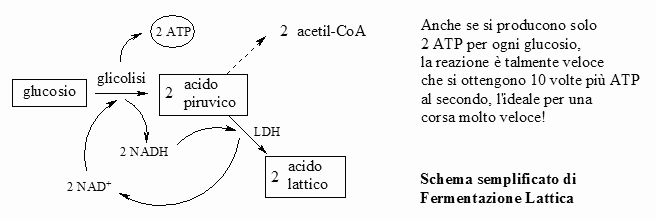 Il prezzo da pagare per eseguire questa reazione è la formazione di acido lattico: nel giro di uno o due minuti la sua concentrazione nei muscoli è così alta che ci costringe a fermarci, ansimando, per recuperare. Il respiro affannoso serve per convertire l'acido lattico in acido piruvico e quindi in glucosio, in una serie di reazioni che avvengono nel fegato e richiedono ossigeno. Il glucosio torna poi alle cellule dove viene convertito in energia in modo aerobico. Mescola e accoppia Le nostre cellule sintetizzano due tipi di lattato deidrogenasi: la forma M e la forma H (esiste anche una terza forma che viene prodotta solo nello sperma). Queste forme sono molto simili per dimensioni e struttura, ma hanno diverse proprietà catalitiche. La forma M, che è la più comune nei muscoli scheletrici, è la migliore per convertire l'acido piruvico in acido lattico. E' sempre pronta ad entrare in funzione se il muscolo deve compiere lavoro anaerobico. La forma H, invece, è la migliore per realizzare la reazione opposta, cioè per convertire l'acido lattico in acido piruvico. E' la forma più comune nel cuore, che ha un costante apporto di ossigeno e quindi può usare l'acido lattico come fonte di energia aerobica. I due tipi hanno una struttura così simile che possono anche formare complessi misti, per esempio con due catene H e due catene M. In questo modo cellule diverse possono costruirsi dei complessi di lattato deidrogenasi su misura a seconda delle loro reali necessità. La molecola mostrata qui all'inizio della pagina (file PDB 3ldh) è la forma con quattro catene M identiche. 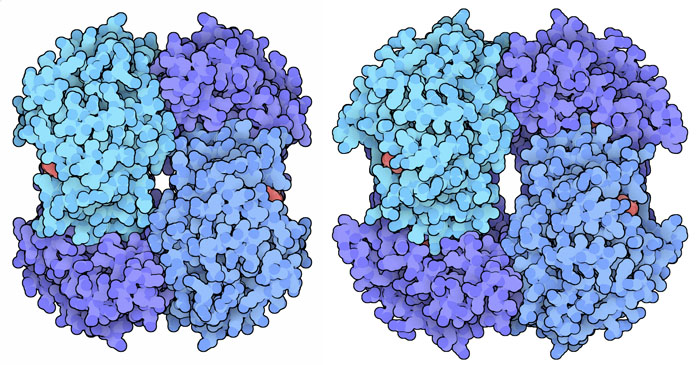 Fermentazione FermentazioneAlcuni batteri ottengono la maggior parte dell'energia dalla conversione del glucosio in acido lattico. Questo processo è chiamato fermentazione lattica e tutti l'abbiamo probabilmente apprezzata in alcuni alimenti. Per trasformare il latte in yogurt, si usano dei batteri fermentanti, inoltre l'acido lattico della fermentazione è uno dei principali componenti del sapore dei crauti e del pane sourdough (un pane americano fermentato anche con enzimi che producono acido lattico). La lattato deidrogenasi batterica mostrata qui a destra (file PDB 1lth) è un enzima allosterico (cioè possiede oltre al sito attivo anche un altro sito di controllo). Il legame con il fruttosio-1,6-difosfato, uno dei primi intermedi della glicolisi, attiva l'enzima facendogli assumere la giusta struttura. La struttura del file PDB 1lth contiene due diverse forme dell'enzima, una attiva, sulla sinistra, l'altra inattiva, sulla destra. Esplorando la struttura I protozoi parassiti che provocano la malaria, durante una fase del ciclo di infezione, utilizzano la fermentazione lattica per ottenere la maggior parte della loro energia. I ricercatori stanno cercando dei farmaci per bloccare la lattato deidrogenasi nel tentativo di attaccare questi parassiti e fermare l'infezione. Le figura qui sotto (file PDB 1cet) mostra una lattato deidrogenasi del parassita Plasmodio della malaria che ha legato quattro molecole di un farmaco antimalarico, clorochina, nei quattro siti attivi. . . . . . . . . 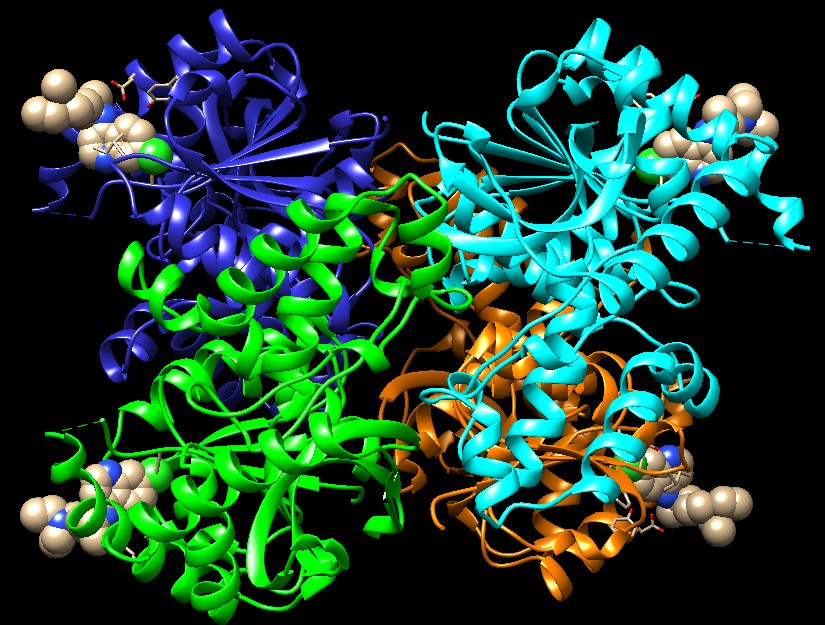 La figura qui sotto è un primo piano della porzione in alto a sinistra della figura precedente. Sono visibili gli amminoacidi che abbracciano la molecola di clorochina nel sito attivo. Cinque sono amminoacidi apolari (verdi) quattro formano la base della tasca di legame ed uno ne disegna il tetto. Ma si notano anche tre amminoacidi polari (rosa), acido aspartico, acido glutammico e tirosina che interagiscono con la parte polare della molecola di clorochina: gli atomi d'azoto (blu) e il cloro (verde). . . . . . . . . . . . . 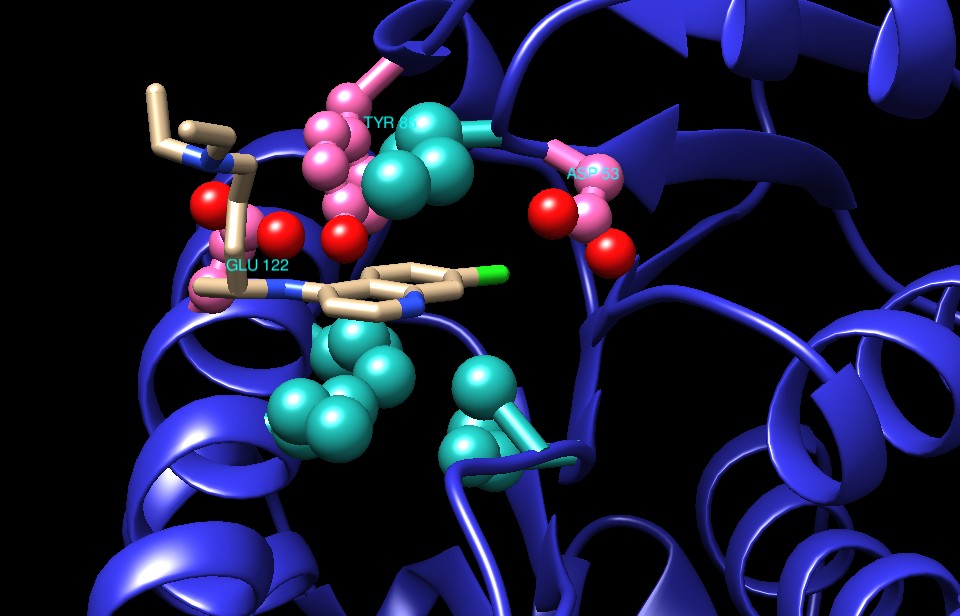 La clorochina, uno dei farmaci più utilizzati per trattare la malaria, ha anche un altro bersaglio, oltre al sito attivo della lattato deidrogenasi. Si pensa che blocchi la via insolita che il parassita utilizza per nutrirsi nel sangue. I ricercatori stanno studiando anche altre molecole anti-malariche che colpiscono la lattato deidrogenasi, come quelle mostrate nei file PDB 1t24, 1t25. D. L. Nelson, M. M. Cox (2000) Lehninger Principles of Biochemistry. Worth Publishers. M. T. Madigan, J. M. Martinko and J. Parker (2000) Brok Biology of Microorganisms. Prentice Hall. J. A. Read, K. W. Wilkinson, R. Tranter, R. B. Sessions and R. L. Brady (1999) Chloroquine binds in the cofactor binding site of Plasmodium falciparum lactate dehydrogenase. Journal of Biological Chemistry 274, 10213-10218. S. Iwata, K. Kamata, S. Yoshida, T. Minowa and T. Ohta (1994) T and R states in the crystals of bacterial L-lactate dehydrogenase reveal the mechanism for allosteric control. Structure 1, 176-185. J. J. Holbrook, A. Liljas, S. J. Steindel and M. G. Rossman (1975) Lactate Dehydrogenase. In "The Enzymes," P. D. Boyer, editor. Academic Press. Volume XI, pages 191-292.
|
||||||
|
|
||||||
