|
|
Citocromo p450 |
|||||
|
Molecola del Mese di Ottobre 2006 Il citocromo p450 rende solubili in acqua i farmaci e le tossine introducendo atomi di ossigeno che ne facilitano l'eliminazione. 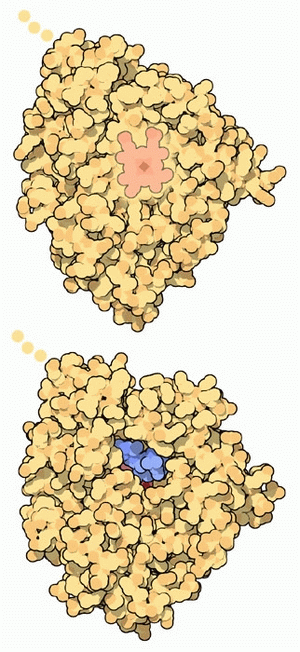 Citocromo
p450 Citocromo
p450Se abbiamo mal di testa e prendiamo un farmaco per combattere il dolore, scopriremo che il suo effetto scompare entro qualche ora. Questo accade perchè abbiamo un sistema di eliminazione delle tossine che individua le sostanze chimiche estranee, come i farmaci, e le espelle dal nostro corpo. Questo sistema combatte tutti i tipi di sostanze chimiche indesiderate che abbiamo assunto per bocca o respirando, compresi i farmaci, i veleni vegetali, le sostanze cancerogene prodotte nel cibo durante la cottura e gli inquinanti presenti nell'ambiente. Gli enzimi citocromo p450 sono la nostra prima linea di difesa in questa battaglia chimica. La seconda linea di difesa è costituita dagli enzimi glutatione tranferasi (mdm 8-2017) che legano un piccolo peptide, il glutatione, alle molecole da espellere per marcarle e poi degradarle. Aggiungere ossigeno Gli enzimi citocromo p450 trovano le molecole estranee e vi aggiungono atomi di ossigeno. Nella maggior parte dei casi, questo ha l'effetto di renderle più solubili in acqua e quindi più facilmente eliminabili dal corpo. L'ossigeno aggiunto diventa un facile punto di aggancio per altri enzimi disintossicanti che così possono afferrare, modificare ulteriormente e distruggere queste molecole tossiche. La strategia di aggiungere ossigeno è chimicamente astuta e gli enzimi citocromo p450 usano uno strumento molecolare potente per realizzarla: l'atomo di ferro di un gruppo eme (file PDB eme). Una strategia alternativa per rendere solubili farmaci e tossine consiste nell'aggiungere alle molecole gruppi solfato come fa l'enzima solfotrasferasi (mdm 8-2009) Citocromo p450 ovunque Gli enzimi citocromo p450 si trovano in tutti gli organismi. Ogni organismo produce molti citocromi p450 diversi, ognuno dei quali agisce su una diversa classe di molecole. I batteri ne hanno circa 20 forme diverse e noi ne abbiamo circa 60. Le piante ne possiedono centinaia, dato che producono molti pigmenti e tossine per difendersi. Molte delle reazioni necessarie per sintetizzare queste molecole vengono realizzate da particolari enzimi citocromo p450. Una lama a doppio taglio La molecola mostrata qui è CYP3A4 (file PDB 1w0e e 2j0d), il citocromo p450 che svolge il ruolo principale nella eliminazione dei farmaci dal nostro corpo. Si stima che questo enzima sia attivo su circa la metà dei farmaci conosciuti. Per esempio, modifica l'antibiotico eritromicina (file PDB eritromicina), mostrato in blu nella figura qui sopra. E' in grado di eliminare farmaci diversi come codeina, diazepam (Valium), paclitaxel (Taxol), e molti farmaci anti-HIV. In alcuni casi, tuttavia, la reazione realizzata dagli enzimi citocromo p450 può essere più dannosa che utile. Per esempio, CYP3A4 è in parte responsabile della tossicità di forti dosi di paracetamolo (Tachipirina). La forma modificata del paracetamolo è pericolosamente reattiva, ma viene normalmente eliminata in breve tempo da altri enzimi disintossicanti. Quando però il dosaggio di paracetammolo è troppo elevato, la concentrazione dell'intermedio reattivo può salire a livelli pericolosi. Prescrizioni e p450 I medici devono tener conto degli enzimi citocromo p450 quando prescrivono dei farmaci. Per esempio, vi sarà capitato di leggere le avvertenze sulle prescrizioni che raccomandano di non bere succo di pompelmo se dovete assumere un certo farmaco. Il pompelmo, infatti, contiene dei flavonoidi che inibiscono gli enzimi citocromo p450. Questo rallenta lo smaltimento dei farmaci che possono produrre così effetti più intensi di quelli che il medico si aspettava. 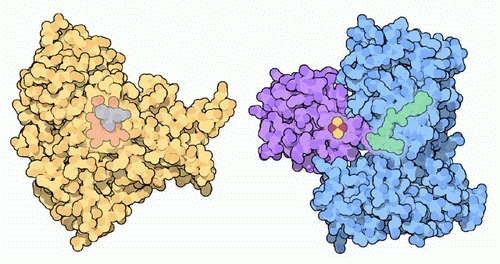 Maghi
della sintesi Maghi
della sintesiGli enzimi citocromo p450 svolgono un ruolo essenziale anche nella sintesi di alcuni normali composti. Per esempio particolari enzimi citocromo p450 realizzano alcuni passaggi della sintesi di steroidi, delle vitamine A e D, e di molecole lipidiche di segnalazione (prostaglandine, trombossani, leucotreni, tutti derivati dell'acido arachidonico). L'enzima mostrato qui a fianco sulla sinistra, è un citocromo p450 di fungo che realizza uno dei passaggi nella sintesi degli steroidi (file PDB 1ea1). Il complesso enzimatico sulla destra fornisce gli elettroni per la reazione (file PDB 1e6e). Un enzima simile al citocromo p450 di fungo, nelle nostre cellule, è necessario per la sintesi del colesterolo. Esplorando la struttura Il citocromo p450 più studiato è un enzima batterico che aggiunge ossigeno alla canfora (file PDB canfora). Due strutture di questo enzima sono illustrate qui sotto. La struttura sulla sinistra (file PDB 3cpp) mostra un enzima avvelenato con monossido di carbonio CO. Notate che, al posto dell'ossigeno O2, sull'atomo di ferro (grossa sfera arancione al centro dell'eme) è legata una molecola di monossido di carbonio. La canfora, legata subito sopra l'eme, non può quindi reagire con l'ossigeno. Questo ci ha permesso di isolare l'enzima con la canfora nel sito attivo prima che avvenga la reazione con l'ossigeno. La struttura sulla destra (file PDB 1noo) illustra un enzima normale e mostra la canfora già ossidata, dopo che ha subito la reazione con l'ossigeno O2. L'atomo di ossigeno che si è sommato alla canfora è quello rosso che si trova sopra il ferro dell'eme. Il secondo atomo di ossigeno della molecola di O2 viene rilasciato come acqua H2O. Le due immagini qui sotto sono state ottenute ottenute con Chimera (vedi chimica al computer). 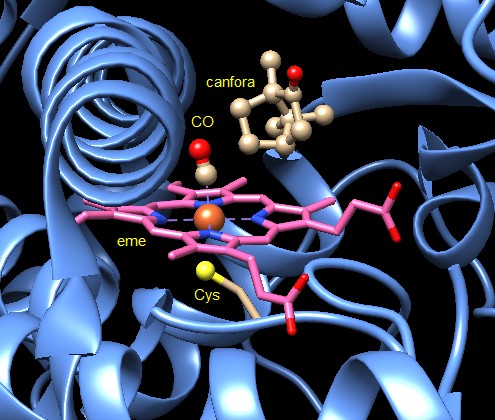
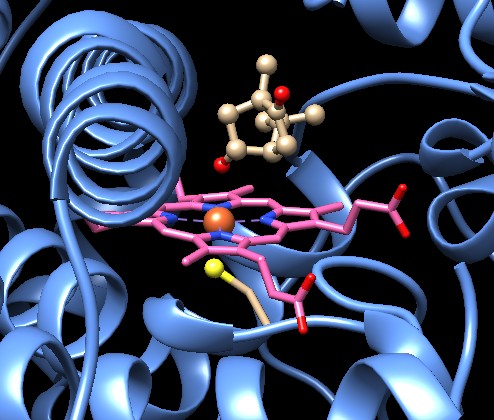 Cercando negli archivi PDB, si possono trovare dozzine di strutture di citocromo p450 che mostrano una varietà di molecole diverse legate nel piccolo sito attivo e che mostrano diversi stadi di reazione. F. P. Guengerich (2001) Common and Uncommon Cytochrome p450 Reactions Related to Metabolism and Chemical Toxicity. Chemical Research in Toxicology 14, 611-650. P. Anzenbacher, E. Anzenbacherova (2001) Cytochromes p450 and Metabolism of Xenobiotics. Cellular and Molecular Life Sciences 58, 737-747. F. P. Guengerich (1993) Cytochrome p450 Enzymes. American Scientist 81 (Sept-Oct), 440-447
|
||||||
|
|
||||||
