|
|
Acetolattato sintasi | |||||
|
Molecola del mese di novembre 2021 Nelle piante l'enzima ALS realizza il primo passaggio nella sintesi dei tre amminoacidi a catena ramificata Val, Ile, Leu e questo lo rende un ottimo bersaglio per gli erbicidi. 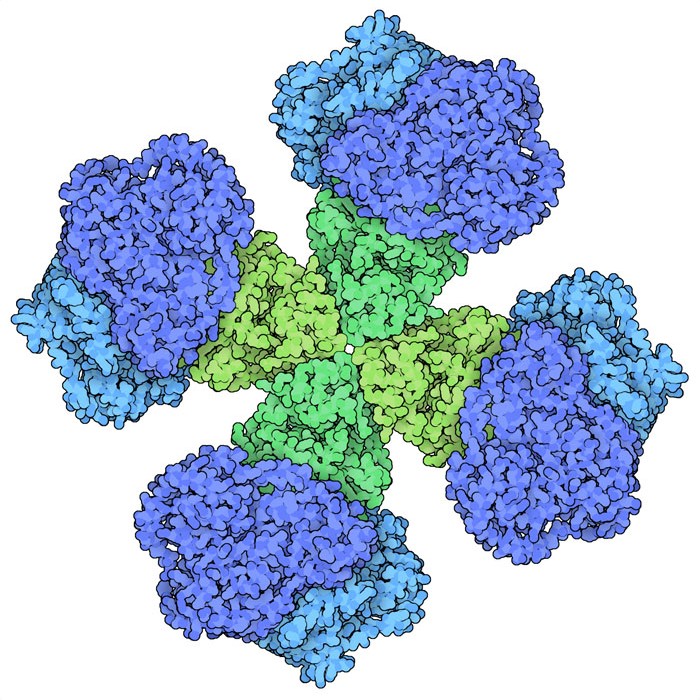 Introduzione IntroduzioneNel corso dell'evoluzione molte funzioni biologiche e biochimiche sono state conquistate e perse. Questo è accaduto per gli organismi, per esempio la selezione naturale ha prodotto farfalle dall'aspetto identico a foglie che, grazie a questo mimetismo, si difendono dai predatori. D'altra parte animali che vivevano in grotte profonde e buie hanno perso progressivamente ogni colore e persino la vista per meglio adattarsi a vivere in un ambiente del tutto buio. Nello stesso modo l'evoluzione agisce anche a livello molecolare. Le piante possiedono tutti i processi molecolari per sintetizzare ogni amminoacido a partire dalle molecole semplici che ottengono dall'ambiente. Gli animali, invece hanno perso questa capacità nel corso dell'evoluzione. Noi stessi otteniamo gli amminoacidi che ci servono nutrendoci di piante o di animali e così le nostre cellule hanno perso la capacità di sintetizzare nove tipi di amminoacidi che oggi chiamiamo amminoacidi essenziali e che dobbiamo assumere con la dieta. Sintetizzare amminoacidi Leucina, isoleucina e valina sono tre amminoacidi essenziali nella nostra dieta. Tutti e tre hanno una catena laterale idrocarburica, cioè formata solo di idrogeno e carbonio, con una piccola ramificazione e sono chiamati amminoacidi a catena ramificata. Le piante, i batteri e i funghi, invece, li possono sintetizzare a partire dall'acido piruvico prodotto dalla glicolisi. L'enzima acetolattato sintasi ALS, chiamato anche acetoidrossiacido sintasi AXAS, (mostrato qui sopra dal file PDB 6vz8) realizza il primo passaggio di questa sintesi. Per formare valina, prende due molecole di acido piruvico, elimina CO2 da una di queste e unisce la parte rimanente al secondo acido piruvico per formare un intermedio nella sintesi dell'amminoacido. In seguito, tre altri enzimi riarrangiano la molecola e aggiungono il gruppo amminico per formare l'amminoacido voluto. Per sintetizzare leucina e isoleucina, il percorso è leggermente diverso, la sintesi inizia legando al primo acido piruvico una molecola un po' più grande del secondo acido piruvico nella reazione catalizzata da ALS. Percorsi sintetici Quando studiamo gli enzimi biosintetici li immaginiamo organizzati in precisi percorsi sintetici lungo i quali le molecole sono modificate passo passo. Spesso in questi percorsi vi è un enzima chiave che realizza un passaggio irreversibile della reazione. Nella sintesi di valina e isoleucina, il passaggio senza ritorno è il primo ed è realizzato dall'enzima ALS. Quando le due molecole di acido piruvico si sono fuse assieme formando l'acido acetolattico, sono obbligate a proseguire nelle reazioni fino alla sintesi della valina. I passaggi irreversibili sono quelli nei quali il processo di biosintesi viene regolato dallo stesso organismo che lo realizza e quindi sono punti vulnerabili che possono bloccare l'intera sintesi se vengono attaccati da opportuni inibitori. L'enzima ALS è il bersaglio di molti dei più comuni erbicidi. E' un bersaglio interessante perchè gli erbicidi che lo colpiscono sono molto efficaci dato che bloccano una via sintetica essenziale per la pianta e inoltre sono relativamente sicuri da usare dato che l'enzima ALS non esiste nelle nostre cellule. Regolare il processo 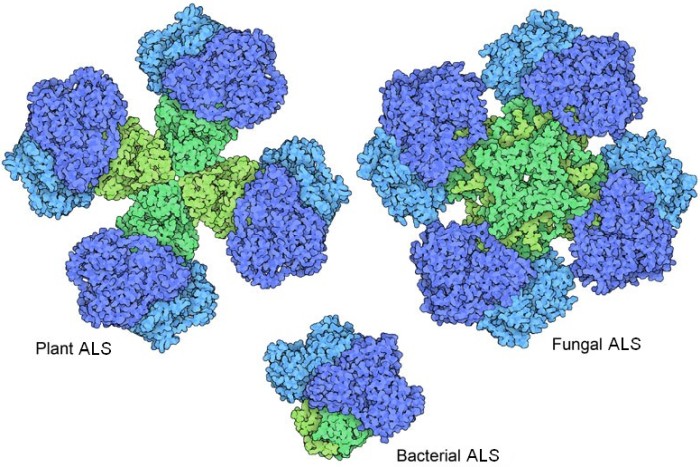 Dato
che l'enzima ALS realizza un passaggio irreversibile nella sintesi degli
amminoacidi a catena ramificata, è l'enzima giusto per regolare
l'attività di questa via enzimatica. In generale gli enzimi ALS
sono composti di due subunità: la subunità catalitica (nei
toni del blu) realizza la reazione, la subunità regolatoria (nei
toni del verde) ne controlla l'azione. Dato
che l'enzima ALS realizza un passaggio irreversibile nella sintesi degli
amminoacidi a catena ramificata, è l'enzima giusto per regolare
l'attività di questa via enzimatica. In generale gli enzimi ALS
sono composti di due subunità: la subunità catalitica (nei
toni del blu) realizza la reazione, la subunità regolatoria (nei
toni del verde) ne controlla l'azione. Quando vi è abbondanza di valina, questa si lega alla subunità regolatoria che modifica la struttura della subunità catalitica rendendola meno attiva e così rallenta la produzione degli amminoacidi a catena ramificata. Quando, invece, i livelli di valina sono bassi, non ce n'è abbastanza per legare la subunità regolatoria e così il complesso torna ad assumere la forma più attiva. Le subunità catalitiche anche se appartengono ad organismi diversi sono molto simili tra loro, mentre le subunità regolatorie sono variabili. Tre di queste sono illustrate qui. L'enzima ALS delle piante (file PDB 6vz8) possiede quattro grosse subunità regolatorie (verdi). L'enzima ALS di fungo (file PDB 6u9d) ha otto subunità regolatorie ognuna con dimensioni metà di quelle delle piante. L'enzima ALS batterico (file PDB 6lpi) ha due subunità regolatorie ed il complesso enzimatico è più piccolo. 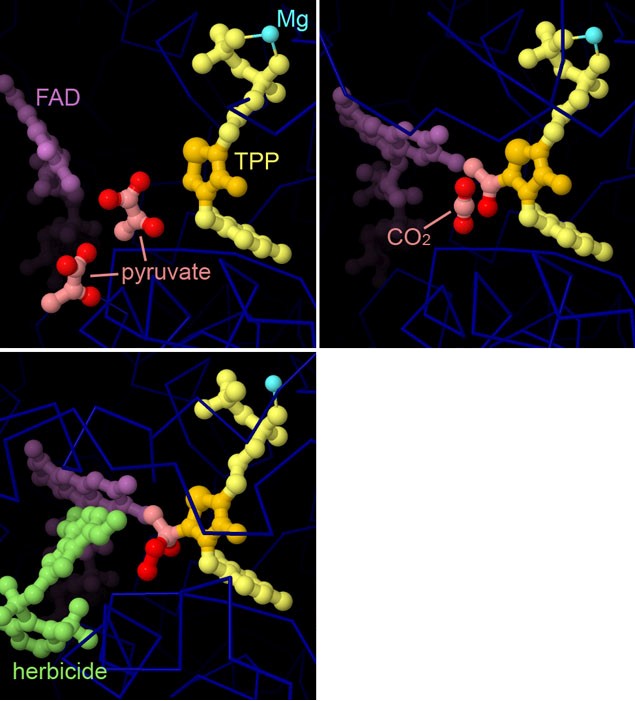 Esplorando
la struttura Esplorando
la strutturaLe seguenti strutture dell'enzima ALS di lievito hanno rivelato i passaggi fondamentali della reazione e hanno chiarito come gli inibitori usati come erbicidi la bloccano. La tiamina-pirofosfato TPP o vitamina B1 (gialla con l'anello reattivo arancione) è il coenzima che aiuta a realizzare la prima parte della reazione che consiste nel rimuovere CO2 dall'acido piruvico. Uno ione magnesio (azzurro) tiene nella corretta posizione il coenzima. L'enzima ALS si lega anche al FAD (viola) nella sua forma ridotta (FADH2) e lega anche quattro molecole di ossigeno O2 dalla funzione non nota (non mostrate qui). Nella prima struttura di ALS qui a lato sulla sinistra (file PDB 6bd9) ci sono due molecole di acido piruvico (rosse e rosa) che stanno entrando nel sito attivo. Nella seconda struttura di ALS qui a lato sulla destra (file PDB 6bd3) una delle molecole di acido piruvico si è legata alla tiamina pirofosfato ed è stata decarbossilata cioè ha perso CO2. La terza struttura di ALS (file PDB 5wkc) ha una molecola di erbicida (penoxulam verde) che blocca l'ingresso al sito attivo. Questa, inoltre, ha provocato l'ossigenazione del substrato che si è trasformato in un perossido cioè una delle molecole di O2 si è legata all'acido piruvico decarbossilato. La molecola che è stata ossigenata (acido perossiacetico rosa e rosso) si può staccare dal coenzima TPP e può ossidare il FADH2 inibendo ulteriormente la reazione enzimatica. In assenza dell'erbicida, nella seconda struttura di ALS qui in alto sulla destra, il frammento decarbossilato (rosa), legato al coenzima TPP, non si lega a O2, ma ad una seconda molecola di acido piruvico formando l'acido acetolattico mostrato qui sotto. La parte in alto a destra della molecola è il frammento decarbossilato, la parte rimanente è il secondo acido piruvico. . . . . . . . . . . . . . . . . . . . . . . . . . . . 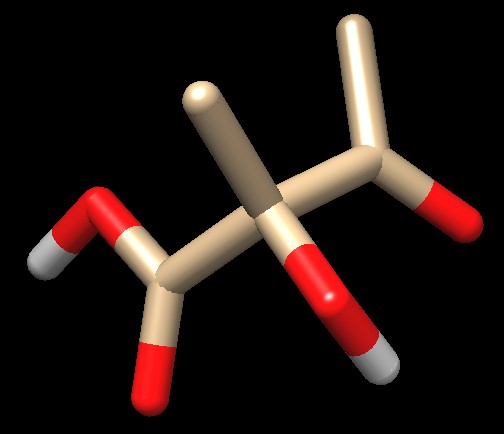 Spunti per ulteriori esplorazioni Diversi erbicidi possono bloccare l'azione dell'enzima ALS. Tutti bloccano l'ingresso dei substrati nel sito attivo, ma hanno strutture diverse e si legano in modi un po' diversi. Fate una ricerca nel sito PDB per ALS o AHAS per trovare queste strutture. Notate che cercando strutture di ALS (o AHLS) negli archivi PDB potreste incontrare complessi con forme diverse. Per esempio, alcune strutture includono solo un dimero della subunità catalitica che si associa per formare tetrameri solo quando lega l'erbicida. Bibliografia 6lpi: Zhang, Y., Li, Y., Liu, X., Sun, J., Li, X., Lin, J., Yang, X., Xi, Z., Shen, Y. (2020) Molecular architecture of the acetohydroxyacid synthase holoenzyme. Biochem J 477: 2439-2449 5wkc: Lonhienne, T., Garcia, M.D., Pierens, G., Mobli, M., Nouwens, A., Guddat, L.W. (2018) Structural insights into the mechanism of inhibition of AHAS by herbicides. Proc Natl Acad Sci U S A 115: E1945-E1954 6bd9, 6bd3: Lonhienne, T., Garcia, M.D., Noble, C., Harmer, J., Fraser, J.A., Williams, C.M., Guddat, L.W. (2017) High resolution crystal structures of the acetohydroxyacid synthase-pyruvate complex provide new insights into its catalytic mechanism. ChemistrySelect, DOI: 10.1002/slct.201702128 Liu, Y., Li, Y., Wang, X. (2016) Acetohydroxyacid synthases: evolution, structure, and function. Appl Microbiol Biotechnol 100: 8633-8649 Gutiérrez-Preciado, A., Romero, H., Peimbert, M. (2010) An evolutionary perspective on amino acids. Nature Education 3(9):29 |
||||||
|
|
||||||
