|
|
Isoprene sintasi |
|||||
|
Molecola del Mese di Settembre 2016 Le piante rilasciano un miliardo di tonnellate di isoprene e di altri gas organici ogni anno. 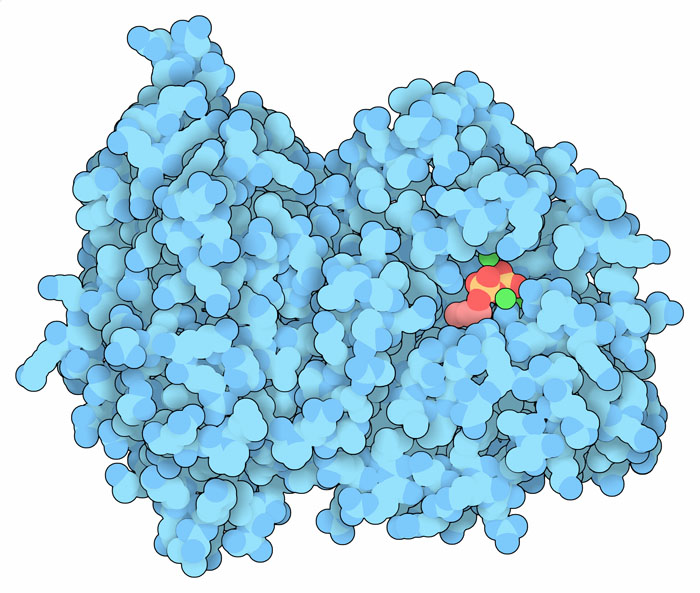 Introduzione IntroduzioneSembra incredibile, ma le piante rilasciano nell'atmosfera un miliardo di tonnellate di sostanze organiche gassose ogni anno. Circa la metà di queste sostanze è costituita da isoprene, . . . . . . 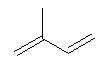 un composto organico gassoso emesso dai grandi alberi, come querce, pioppi ed eucalipti che sono abbondanti nelle foreste di tutto il mondo. La quantità di isoprene emesso è così grande che filtra la luce solare e forma quella leggera foschia azzurrina che rende affascinanti i panorami (si pensi alle Blue mountains in Australia). Rilasciare isoprene Le piante producono isoprene con l'enzima isoprene sintasi mostrato qui a fianco (file PDB 3n0g). Questo enzima rompe la molecola di dimetil-allil-difosfato (DMAPP), 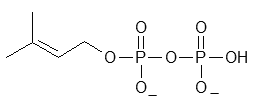 ed, eliminando i due fosfati, forma isoprene. 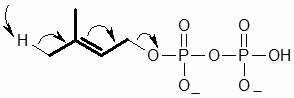 Isoprene è il materiale di partenza per la sintesi di molte molecole isoprenoidi come il limonene, il beta-carotene o il colesterolo, una famiglia di molecole molto vasta, in natura, che comprende circa 55.000 molecole diverse. L'enzima isoprene sintasi usa ioni magnesio (mostrati in verde nella figura) per rimuovere il difosfato dal DMAPP (in rosa, rosso e giallo) e formare i due doppi legami dell'isoprene. Questo svolge un ruolo importante nella chimica dell'atmosfera. Si è scoperto, per esempio, che reagisce con i radicali idrossido e con gli ossidi d'azoto nell'aria contribuendo ad innalzare la concentrazione di ozono. La comprensione del meccanismo di azione della isoprene ossidasi sta permettendo ai ricercatori di ingegnerizzare nuove forme dell'enzima per sintetizzare isoprene da usare come materiale di partenza per la produzione industriale di gomme e polimeri. Proteggere le foglie Le foglie esposte alla luce solare diretta si scaldano molto in superficie e quindi si pensa che l'isoprene abbia la funzione di proteggerle dalle molecole reattive che si formano col calore. Vi sono molte prove a sostegno di questa ipotesi, per esempio la produzione di isoprene nelle piante non è costante durante l'anno, ma varia con le stagioni e inoltre le foglie sulla cima degli alberi, che sono maggiormente esposte alla luce, ne producono di più. Si è visto poi che le piante emettono isoprene anche in assenza di luce, seppure a bassi livelli, quindi si pensa che l'isoprene agisca anche come meccanismo di difesa per allontanare gli erbivori o per ridurre lo stress della siccità. 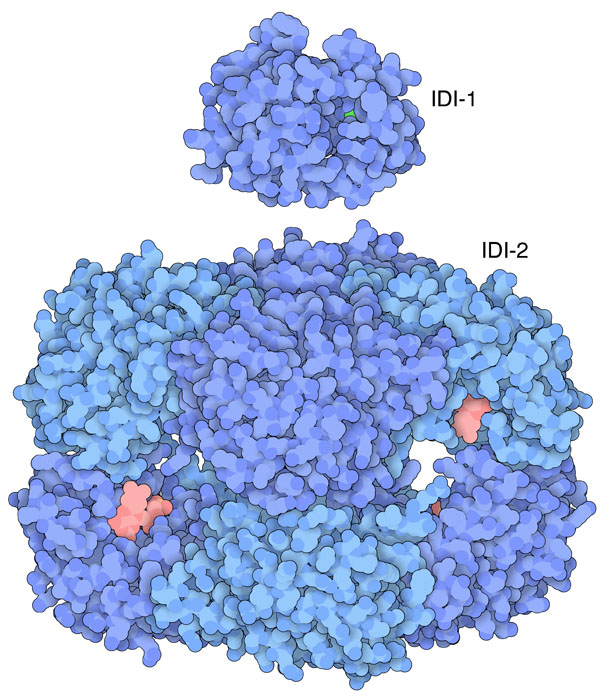 Mattoni
fondamentali Mattoni
fondamentaliSia il precursore dell'isoprene, DMAPP, che un'altra molecola molto simile, isopentenil-difosfato (IPP), 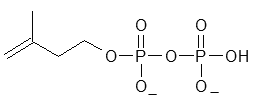 possono essere usate per sintetizzare isoprene e, da questo, costruire molte molecole importanti in tutti gli esseri viventi, dagli ormoni steroidei ai trasportatori di elettroni come l'ubichinone. Le due molecole sono interscambiabili, infatti, a seconda di quale delle due è richiesta, DMPP e IPP vengono interconvertite una nell'altra da un enzima isomerasi. In natura si trovano due forme di questo enzima. L'isomerasi di tipo 1 mostrata qui a fianco in alto (file PDB 1i9a) usa un metallo (manganese, in verde) per catalizzare l'interconversione. L'isomerasi di tipo 2, mostrata qui a fianco in basso (file PDB 1p0n), usa un cofattore nucleotidico (FMN, in rosa) per realizzare la stessa reazione. Esplorando la struttura 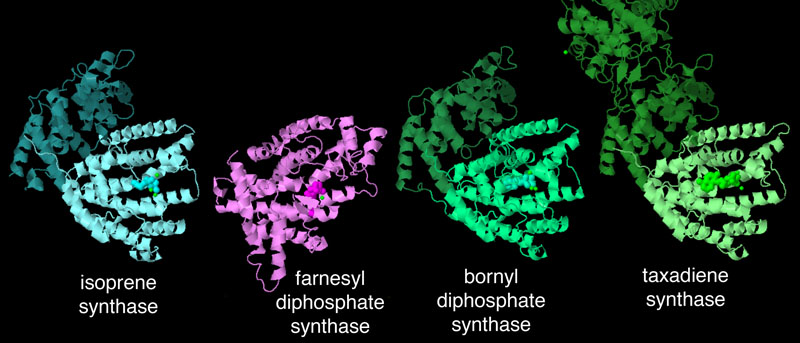 Vi
sono molti enzimi che usano DMAPP e IPP per la sintesi di molecole terpenoidi.
Molti di questi, compresa isoprene sintasi, hanno una struttura caratteristica
formata da 10 alfa-eliche (in evidenza qui a fianco) chiamata "ripiegamento
di terpenoidi sintasi" che costituisce il sito attivo dell'enzima. Vi
sono molti enzimi che usano DMAPP e IPP per la sintesi di molecole terpenoidi.
Molti di questi, compresa isoprene sintasi, hanno una struttura caratteristica
formata da 10 alfa-eliche (in evidenza qui a fianco) chiamata "ripiegamento
di terpenoidi sintasi" che costituisce il sito attivo dell'enzima.
Qui a fianco ne sono mostrati quattro esempi. La prima è isoprene sintasi, che stacca i gruppi fosfato e rilascia isoprene. La seconda è Farnesil difosfato sintasi (file PDB 1fps), che lega tra loro tre unità isopreniche per formare una catena più lunga. La terza è Bornil difosfato sintasi (PDB entry 1n20), che forma degli anelli usando catene di due unità isopreniche. La quarta è Taxadiene sintasi (file PDB 3p5p), che sintetizza strutture più complesse partendo da unità isopreniche per la sintesi del tassolo. Spunti per ulteriori esplorazioni Le molecole isoprenoidi hanno una forma caratteristica con una catena a zig-zag di atomi di carbonio e piccole ramificazioni di un carbonio lungo la catena. Per vederne qualche esempio significativo esaminate la pagina PDB del farnesil difosfato o cercate molecole come clorofilla, beta-carotene, retinolo con "Chemical Component Search" per esplorare le strutture di queste molecole. Questi enzimi spesso usano ioni magnesio nel sito attivo, provate a scoprire qual è il ruolo di questi ioni. F. Loreto, S. Fineschi (2015) Reconciling functions and evolution of isoprene emission in higher plants. New Phytologist 206, 578-582. H. Fuchs, A. Hofzumahaus, F. Rohrer, B. Bohn, T. Brauers, H. P. Dorn, R. Haseler, F. Holland, M. Kaminski, X. Li, K. Lu, S. Nehr, R. Tillmann, R. Wegener & A. Wahner (2013) Experimental evidence for efficient hydroxyl radical regeneration in isoprene oxidation. Nature Geoscience 6, 1023-1026. A. B. Guenther, X. Jiang, C. L. Heald, T. Sakulyanontvittaya, T. Duhl, L. K. Emmons & X. Wang (2012) The model of emissions of gases and aerosols from nature version 2.1 (MEGAN2.1): an extended and updated framework for modeling biogenic emissions. Geoscientific Model Development 5, 1471-1492. 3p5p: M. Koksal, Y. Jin, R. M. Coates, R. Croteau & D. W. Christianson (2011) Taxadiene synthase structure and evolution of modular architecture in terpene biosynthesis. Nature 469, 116-120. 3n0g: M. Koksal, I. Zimmer, J. P. Schnitzler & D. W. Christianson (2010) Structure of isoprene synthase illuminates the chemical mechanism of teragram atmospheric carbon emission. Journal of Molecular Biology 402, 363-373 T. D. Sharkey, A. E. Wiberley & A. R. Donohue (2008) Isoprene emission from plants: why and how. Annals of Botany 101, 5-18. 1p0n: S. Steinbacher, J. Kaiser, S. Gerhardt, W. Eisenreich, R. Huber, A. Bacher & F. Rohdich (2003) Crystal structure of the type II isopentenyl diphosphate:dimethylallyl diphosphate isomerase from Bacillus subtilis. Journal of Molecular Biology 329, 973-982. 1n20: D. A. Whittington, M. L. Wise, M. Urbansky, R. M. Coates, R. B. Croteau & D. W. Christianson (2002) Bornyl diphosphate synthase: structure and strategy for carbocation manipulation by a terpenoid cyclase. Proceedings of the National Academy of Science USA 99, 15375-15380. 1i9a: J. B. Bonanno, C. Edo, N. Eswar, U. Pieper, M. J. Romanowski, V. Ilyin, S. E. Gerchman, H. Kycia, F. W. Studier, A. Sali & S. K. Burley (2001) Structure genomics of enzymes involved in sterol/isoprenoid biosynthesis. Proceedings of the National Academy of Science USA 98, 12896-12901. 1fps: L. C. Tarshis, M. Yan, C. D. Poulter & J. C. Sacchettini (1994) Crystal structure of recombinant farnesyl diphosphate synthase at 2.6-A resolution. Biochemistry 33, 10871-10877. F. W. Went (1960) Blue Hazes in the atmosphere. Nature 187, 641-643.
|
||||||
|
|
||||||
