|
|
Actinomicina |
|||||
|
Molecola del Mese di Aprile 2013 Alcuni antibiotici attaccano le cellule intercalandosi tra le basi del DNA a doppia elica e sono usati come farmaci antitumorali 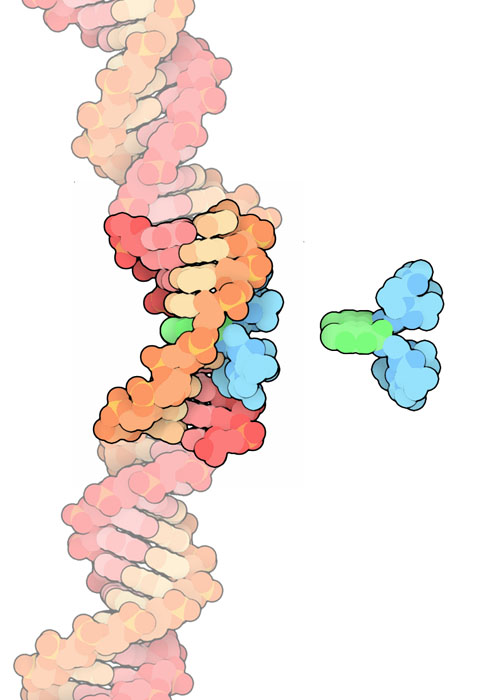 Introduzione IntroduzioneLe cellule sono bravissime nel sintetizzare molecole, e spesso la ricerca di nuovi farmaci comincia proprio da composti trovati in natura. Molti antibiotici sono stati scoperti studiando la guerra continua tra batteri e funghi ed isolando le molecole tossiche che questi producono per combattersi. L'actinomicina è stato il primo antibiotico naturale scoperto che possedeva anche proprietà anticancro. E' stata isolata dal batterio Streptomyces antibioticus nel 1940. Sfortunatamente era troppo tossica per essere usata perchè, mentre uccideva le cellule cancerose, avvelenava anche il paziente. In seguito sono state sviluppate delle varianti della molecola originale che sono ancora oggi molto usate nelle terapie antitumorali. Intercalare il DNA Già dai primi studi sulla actinomicina si è capito che si intercala nella doppia elica del DNA. L'actinomicina è mostrata qui a destra in azzurro e verde (file PDB 173d). E' composta di due parti, un anello piatto (mostrato in verde) che somiglia alle basi azotate del DNA, e due peptidi ciclici formati di amminoacidi insoliti (mostrati in azzurro). L'anello piatto si intercala tra le basi azotate del DNA nella doppia elica e i peptidi ciclici si inseriscono perfettamente nella scanalatura minore del DNA. Il risultato è un complesso stabile e letale per il genoma della cellula. Colpire la topoisomerasi I farmaci intercalanti sono usati nella chemioterapia anti-cancro perchè avvelenano le cellule che si moltiplicano velocemente, come quelle di un tumore. Lo studio di questi farmaci ha rivelato che gli enzimi topoisomerasi (mdm 1-2006) sono il loro principale bersaglio. Le topoisomerasi iniziano la loro azione tagliando la catena del DNA (le topoisomerasi I tagliano una singola catena, le topoisomerasi II tagliano la doppia elica ) poi aumentano o diminuiscono il super avvolgimento della catena facendo passare un tratto della catena attraverso il taglio e infine riconnettono la catena tagliata. I farmaci intercalanti impediscono la riconnessione bloccando la topoisomerasi dopo la fase in cui ha tagliato il DNA. Questo si rivela disastroso per una cellula che deve duplicarsi: quando la forcella di replicazione raggiunge quel punto e gli enzimi che svolgono il DNA passano sopra il tratto danneggiato, e così si ha una rottura letale della doppia elica. 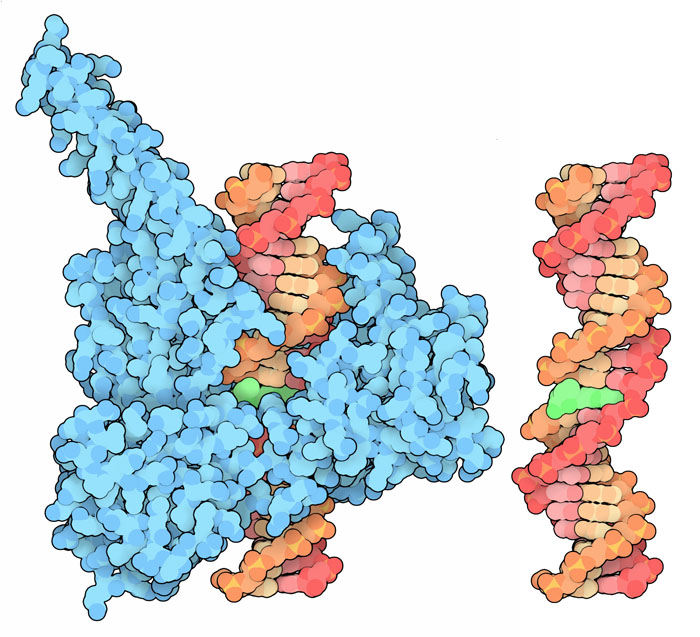 Intercalanti in azione Sono state scoperte molte molecole intercalanti sia ottenute da organismi viventi che sintetizzate in laboratorio. A seconda della loro forma e dimensione attaccano tipi diversi di topoisomerasi. L'actinomicina blocca la topoisomerasi di tipo II che ha la funzione di risolvere l'aggrovigliamento del DNA. La molecola mostrata qui a fianco, un topotecano (verde), invece, blocca le topoisomerasi di tipo I che hanno la funzione di rilassare i super-avvolgimenti del DNA (file PDB 1k4t). La struttura mostra il farmaco (verde) intercalato nel DNA. Questo ha un filamento tagliato ed è legato all'interno della topoisomerasi (grossa proteina azzurra). Esplorando la struttura Molte molecole intercalanti sono generiche e non hanno una preferenza per un tratto specifico di DNA, l'actinomicina, invece, si lega all'interno di una sequenza GC. L'actinomicina mostrata qui sotto (file PDB 173d) è legata ad un breve tratto di DNA e ha rivelato la ragione di questa preferenza: le porzioni della molecola costituite dai peptidi ciclici (azzurre) formano specifici legami idrogeno con i bordi delle due basi di guanina delle due coppie G-C e C-G tra le quali si è intercalata. Questi legami sono rappresentati da sottili linee tratteggiate nelle due figure qui sotto. . . .. . . 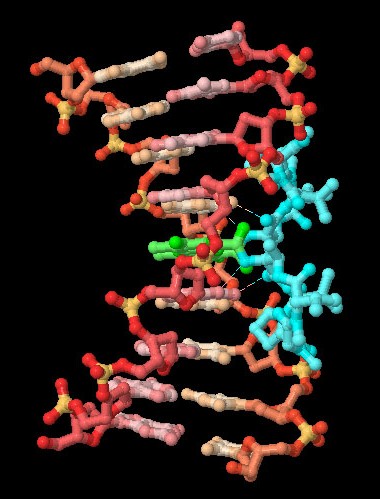 . . .
. . . 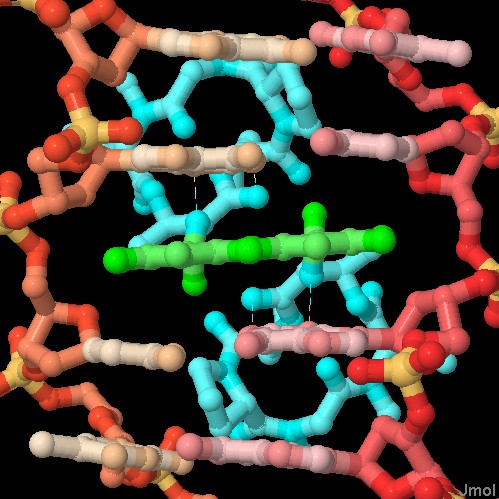
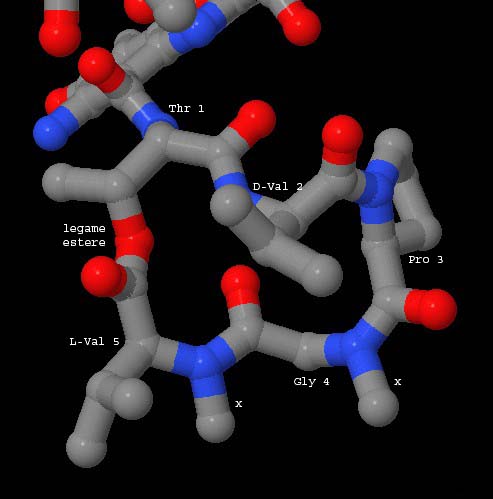
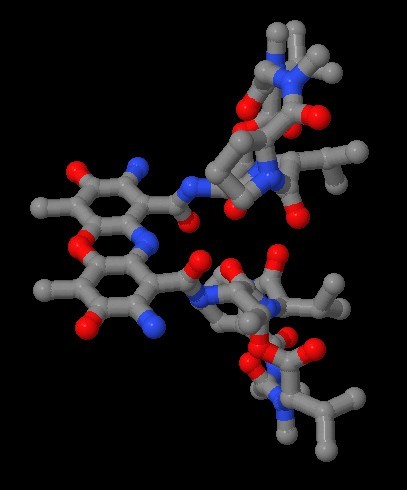
Qui sotto a sinistra è mostrata la molecola dell'actinomicina
senza il DNA. Si vede in dettaglio l'anello intercalante. Ha una struttura
piana ed è composto di tre anelli, così può sovrapporsi
in modo efficace tra le coppie di basi azotate del DNA che sono composte
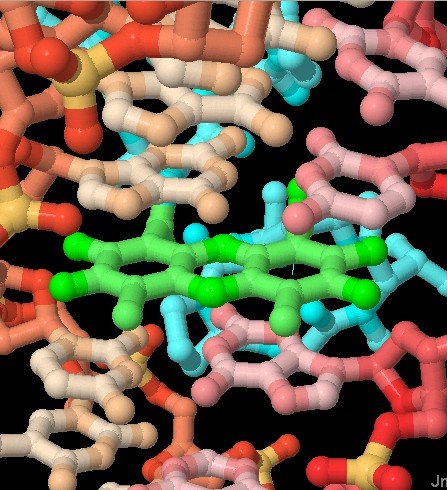
una di due anelli e l'altra di uno solo. La sovrapposizione tra l'anello
intercalante e le basi azotate è mostrata in dettaglio nell'immagine
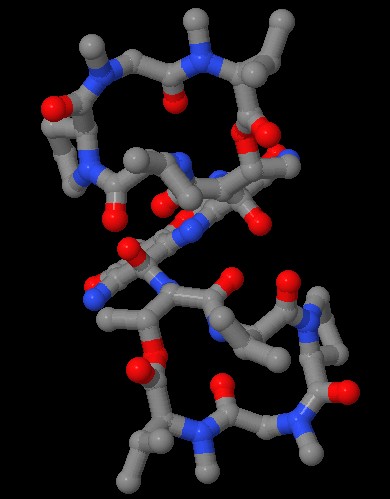
qui sotto a destra. Qui sotto sono mostrati in dettaglio
i due peptidi ciclici dell'actinomicina. Guardando con attenzione si
possono notare alcune stranezze. L'amminoacido treonina 1 (Thr 1) è
legato con il gruppo amminico (blu, verso l'alto) all'anello intercalante,
inoltre è legato con il carbossile (verso destra) al successivo
amminoacido (D-Val 2), e con il gruppo OH in catena laterale (rosso,
verso sinistra) forma un legame estere con la valina 5 (L-Val
5) per chiudere l'anello di amminoacidi.
|
||||||
|
|
||||||

 . . .
. . . 
 . . .
. . .