|
|
ATP sintasi |
|||||
|
Molecola del Mese di Dicembre 2005 L'ATP sintasi è un motore molecolare ed è l'enzima finale della fosforilazione ossidativa che produce ATP sfruttando una differenza di pH 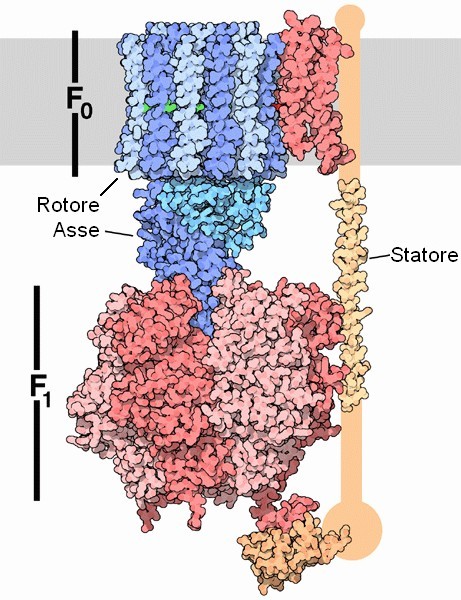 Introduzione IntroduzioneL'ATP sintasi è una delle meraviglie del mondo molecolare. L'ATP sintasi è un enzima, un motore molecolare, una pompa ionica, ed un altro motore molecolare tutti legati insieme in una macchina incredibile dalle dimensioni nanometriche. Ha un ruolo importante nelle nostre cellule dato che sintetizza la maggior parte dell'ATP che dà energia ai processi cellulari. Il meccanismo col quale agisce è sorprendente. Motori rotanti La sintesi di ATP viene realizzata da due motori rotanti, ognuno alimentato da un combustibile diverso. Il primo motore, chiamato Fo, assomiglia ad un motore elettrico, è immerso nella membrana interna dei mitocondri (striscia grigia), ed è mosso dal flusso di protoni (ioni H+) che attraversano la membrana dall'alto verso il basso. Quando i protoni fluiscono attraverso il motore Fo, fanno girare il rotore cilindrico (blu e azzurro) che ruota insieme con un'asse che si inserisce nel secondo motore, chiamato F1. Il secondo motore, F1, è spinto da ATP, ed è vincolato sttraverso uno statore alla parte fissa di Fo (rossa). Quando il rotore di Fo gira, fa girare l'asse all'interno di F1 e, dato che l'asse è un pò eccentrica, questo provoca in F1 una deformazione ciclica. Da motore a generatore Perché avere due motori connessi insieme? Il motivo è che un motore può costringere l'altro a girare, ed in questo modo lo trasforma da motore a generatore. Questo è quello che accade nelle nostre cellule: il motore Fo usa l'energia di un gradiente di protoni per costringere il motore F1 a generare ATP. Nelle nostre cellule, il cibo viene degradato e usato per creare un grande eccesso di ioni idrogeno nello spazio intermembrana dei mitocondri grazie ai complessi della catena di trasporto degli elettroni (mdm 12/2011). La subunità Fo di ATP sintasi permette a questi ioni H+ di tornare nello spazio più interno del mitocondrio, facendo girare il rotore in questo processo. Quando il rotore gira, fa girare l'asse all'interno di F1 e così lo mette in funzione facendolo diventare un generatore che produce ATP. Parti diverse E' molto difficile determinare la struttura tridimensionale di macchine molecolari grandi e complesse come l'enzima ATP sintasi, così la loro struttura viene spesso determinata per parti. La figura mostrata qui sopra è composita, è formata da quattro strutture PDB diverse, alcune determinate con la cristallografia a raggi X, altre con la spettroscopia NMR. Il motore Fo è stato preso dal file PDB 1c17. Il motore F1 e l'asse che connette i due motori sono stati presi dal file PDB 1e79. Lo statore si è dimostrato la parte più elusiva. I due pezzi mostrati qui sono stati presi dai file PDB 2a7u e 1l2p. Esplorando la struttura di Fo Il motore protonico Fo (file PDB 1c17) è mostrato qui sotto visto di lato. E' formato da un cilidro di 12 catene ripiegate a metà per formare due tratti ad alfa elica, e da una tredicesima catena (rossa), la pompa protonica, ripiegata in modo da formare quattro tratti ad alfa elica. Al centro delle catene del cilindro vi sono 12 amminoacidi di acido aspartico (rossi), mentre nella tredicesima catena vi è un'arginina (blu) che si inserisce tra le alfa eliche del cilindro per interagire con gli acidi aspartici del cilindro in rotazione. . . . . . . 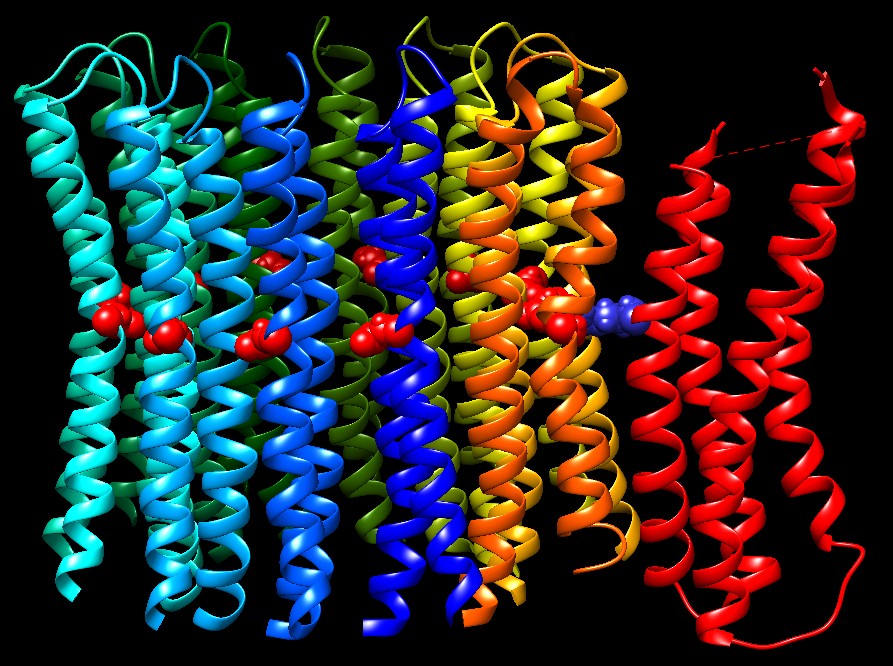 Nella figura seguente si vede il motore Fo lungo l'asse di rotazione. La pompa protonica ha un amminoacido di arginina (blu) che cede uno ione idrogeno agli aspartati del rotore. Gli amminoacidi di aspartato hanno una carica negativa, ma poichè il rotore è immerso nei lipidi della membrana interna dei mitocondri, questa carica negativa è molto sfavorevole. Quindi, il rotore gira per permettere agli aspartati di legarsi agli ioni idrogeno diventando acidi aspartici neutri. Gli ioni idrogeno quindi seguono un percorso circolare attraverso il motore Fo e fanno girare il rotore al loro passaggio. . . . . . 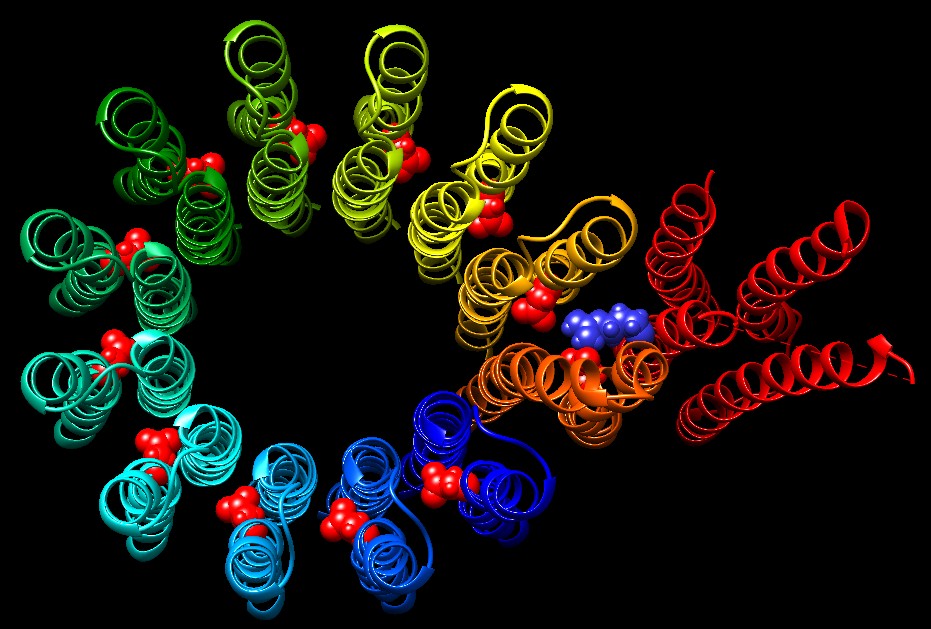 Gli ioni H+ vengono presi dallo spazio intermembrana del mitocondrio (in alto) da una catena di amminoacidi della pompa (rossa), e trasferiti all'arginina. L'arginina passa gli ioni idrogeno agli aspartati del rotore il quale così gira. Poi gli ioni idrogeno vengono ceduti ad altri amminoacidi della pompa, e trasferiti finalmente nella parte più interna del mitocondrio dove gli H+ sono in difetto. Il percorso esatto degli ioni idrogeno attraverso la pompa non è però ancora del tutto chiarito. Gli ioni H+ non possono passare nel foro all'interno del cilindro perchè questo è sigillato da dodici arginine (positive), una per catena, all'imboccatura del cilindro. Nell'immagine qui sotto sono mostrate tutte le arginine (basiche, positive) presenti in Fo. . . . . . . . . 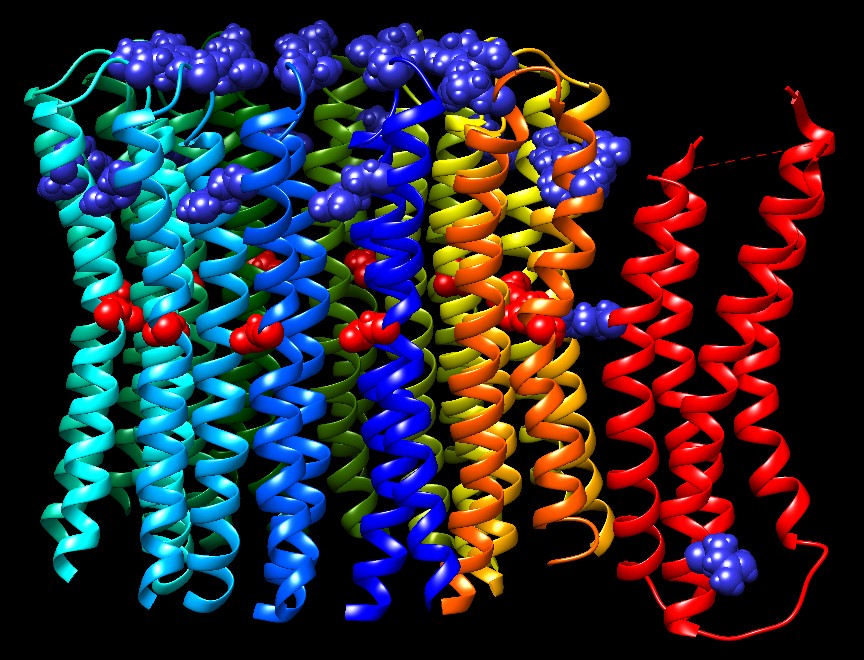 .
. Esplorando
la struttura di F1 Esplorando
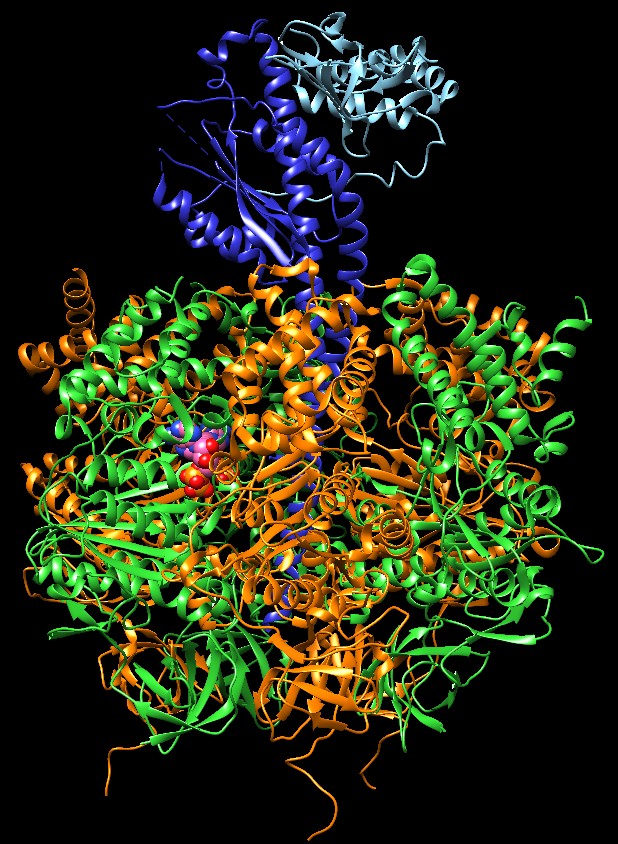
la struttura di F1 Il file PDB 1e79 mostrato qui a fianco contiene il motore F1 dell'ATP sintasi (spicchi verdi e arancioni) e anche l'asse che ruota dentro di lui (blu e azzurro). Quando opera come generatore, usa l'energia del moto di rotazione di Fo per costruire ATP. Quando opera come motore, rompe ATP per ruotare l'asse nella direzione opposta. Il motore F1 ha la forma di un'arancia a sei spicchi. I tre spicchi chiamati alfa (arancioni) hanno funzione strutturale e sono intercalati dai tre spicchi beta (verdi) nei quali avviene la reazione di sintesi di ATP. Questa, infatti, avviene in tre passaggi in ogni spicchio beta, durante la rotazione dell'asse: 1) fissaggio di ADP e fosfato inorganico, 2) formazione di un nuovo legame fosfato-fosfato per generare ATP, 3) rilascio di ATP. 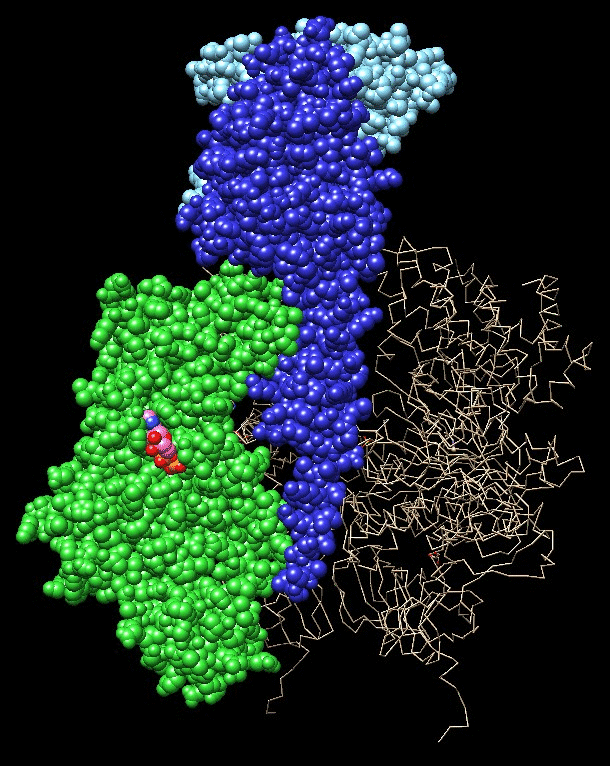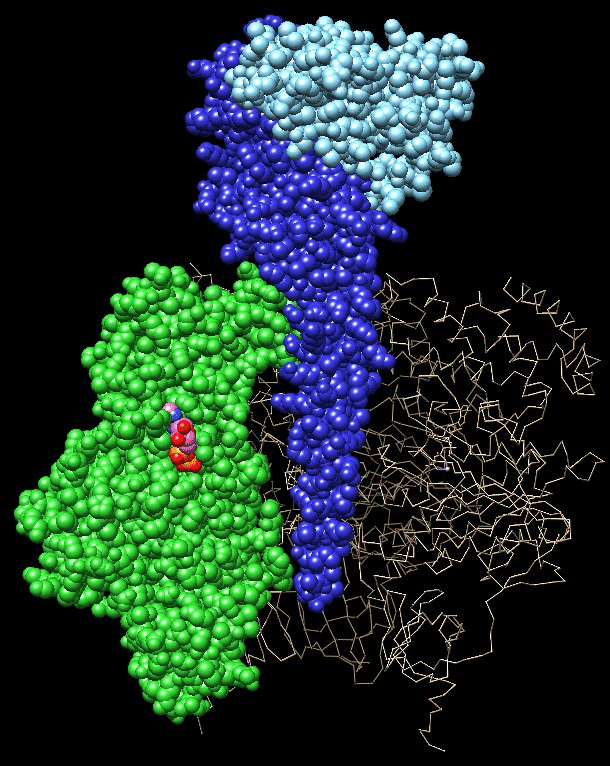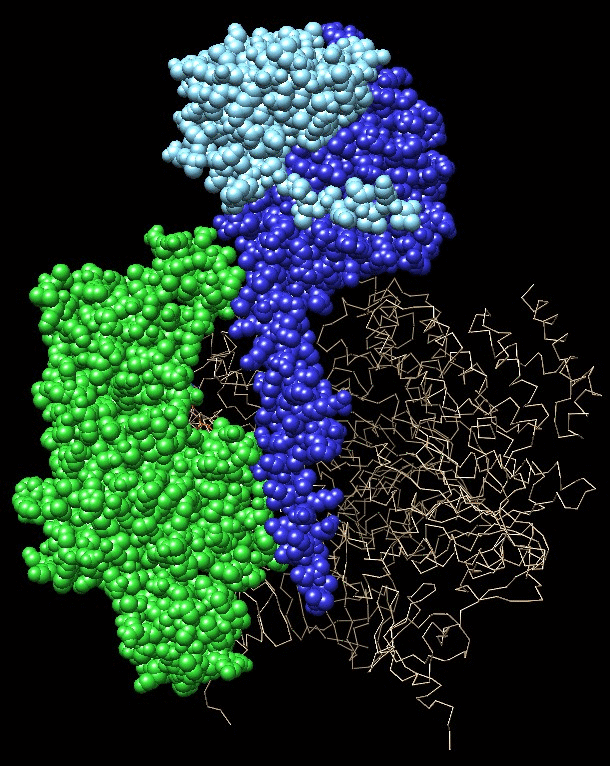 Il
passaggio difficile della reazione è il rilascio di ATP che, per
essere spinto fuori dalla molecola, richiede una particolare deformazione
ben visibile nell'animazione mostrata più a fianco. Il
passaggio difficile della reazione è il rilascio di ATP che, per
essere spinto fuori dalla molecola, richiede una particolare deformazione
ben visibile nell'animazione mostrata più a fianco.Quando l'asse ruota, costringe gli spicchi beta (verdi) del motore F1 ad assumere tre conformazioni diverse che aiutano a realizzare i tre passaggi. La prima e la seconda sono simili, mentre la terza conformazione è molto più aperta. La prima conformazione, più chiusa, fissa ADP (rosa) e un fosfato inorganico. La seconda conformazione favorisce il legame fosfato-fosfato e genera ATP. La terza conformazione è costretta ad aprirsi dalla rotazione dell'asse eccentrico e rilascia ATP. Per meglio comprendere il movimento dell'ATP sintasi guardate questa aninazione che include anche la catena respiratoria. P. D. Boyer (1997) The ATP Synthase: A Splendid Molecular Machine. Annual Review of Biochemistry 66, 717-749. G. Oster and H. Wang (1999) ATP Synthase: Two Motors, Two Fuels. Structure 7, R67- R72. G. Oster and H. Wang (2003) Rotary Protein Motors. Trends in Cell Biology 13, 114- 121.
|
||||||
|
|
||||||
