|
Molecola del mese di gennaio 2000
La mioglobina è stata la prima proteina di cui è stata determinata
la struttura, fissa l'ossigeno che deve essere usato nei muscoli
 La
prima proteina La
prima proteina
Qualsiasi discussione sulla struttura
delle proteine deve cominciare necessariamente con la mioglobina,
perché è stata la prima proteina di cui si è determinata la
struttura.
John Kendrew e il suo gruppo, dopo anni di intenso lavoro, hanno determinato
la struttura atomica della mioglobina ponendo così le fondamenta per
una nuova era di comprensione della biologia.
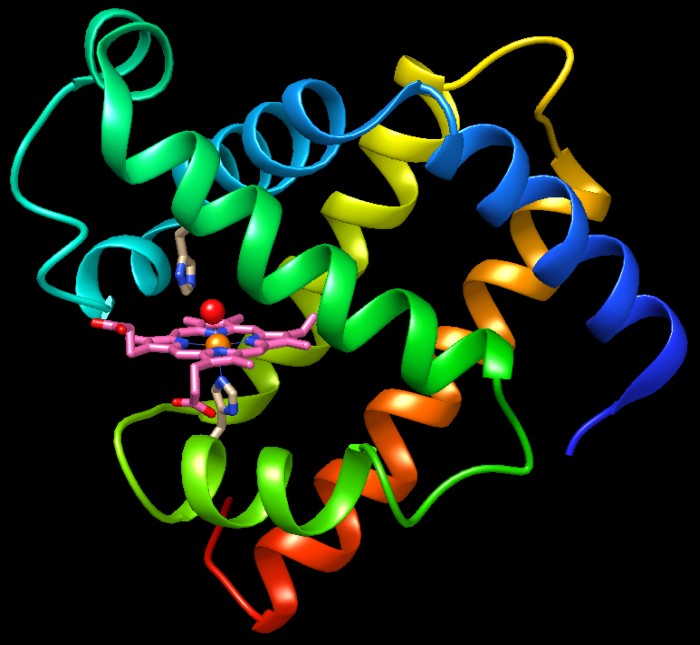
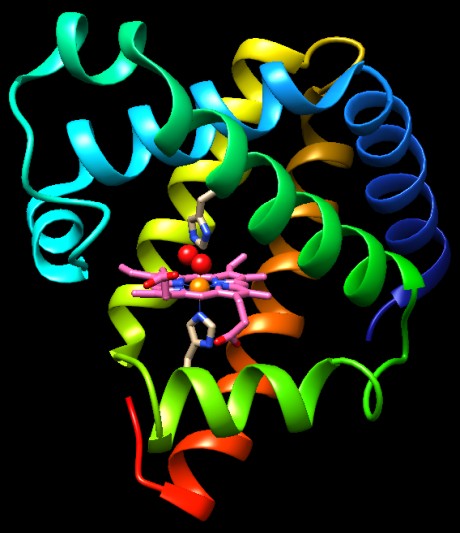
Questa struttura storica è mostrata nelle due immagini
qui a fianco e qui sotto (file PDB 1mbn). Se osservate nel dettaglio questa molecola,
ne rimarrete affascinati, proprio come lo fu il mondo nel 1960, nel
vedere per la prima volta il meraviglioso intreccio di una proteina.
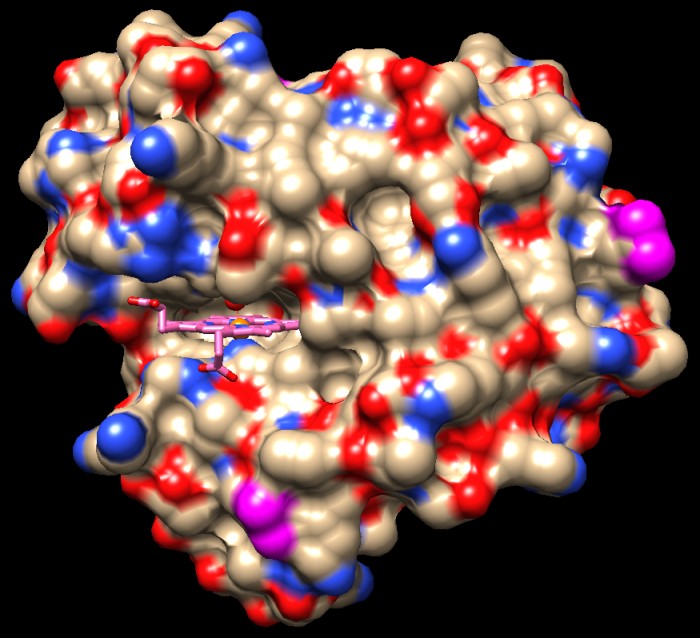 Mioglobina e muscoli
Mioglobina e muscoli
La mioglobina è una proteina piccola e rossa. È
molto comune nelle cellule muscolari e dà alla carne il caratteristico
colore rosso. Il suo compito è immagazzinare ossigeno O2,
che viene usato quando i muscoli devono contrarsi intensamente. Per
fare questo usa uno strumento chimico molto particolare, il gruppo
eme, che le consente di catturare le sfuggenti molecole di ossigeno.
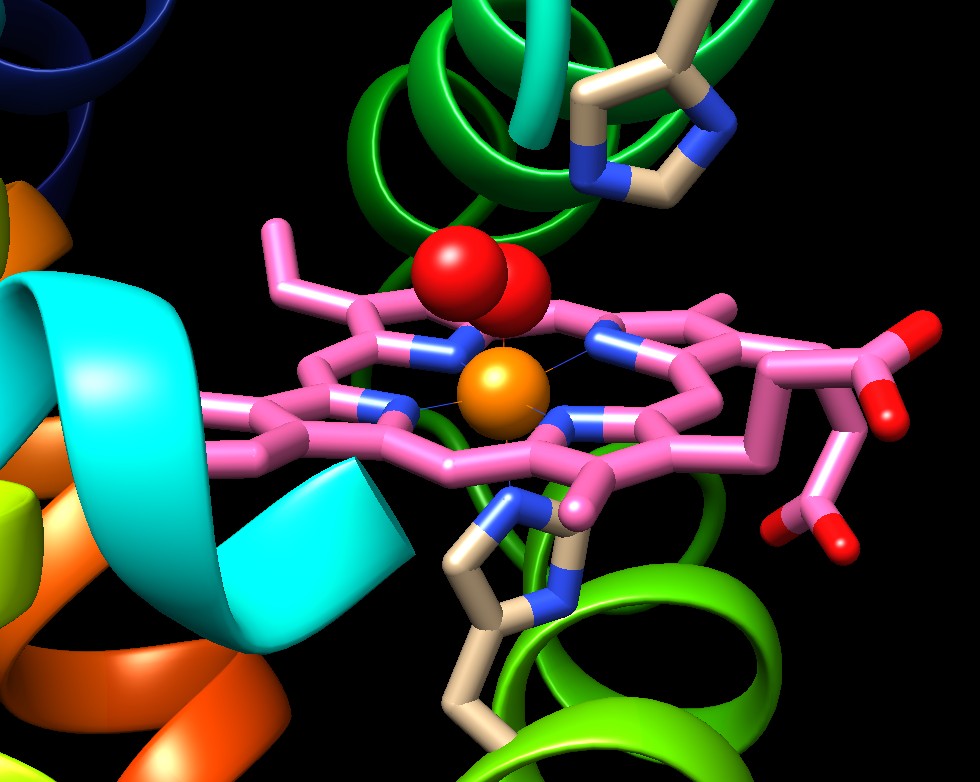
L'eme è una molecola a forma di disco, mostrata in rosa nelle
due figure qui sopra e a lato. Ha un foro al centro dove lega un atomo
di ferro (arancione) ed è questo che riesce a legare l'ossigeno
O2. In realtà,
in questa molecola, il ferro dell'eme non sta legando i due atomi di
ossigeno della molecola O2,
ma lega un singolo atomo di ossigeno (rosso) di una molecola d'acqua.
Questo è comunque sufficiente per darci un'idea della posizione
che assume O2
quando si lega all'eme.
Il gruppo eme si trova in una tasca sottile e profonda sul fianco della
proteina, trattenuto in posizione da due istidine (amminoacidi con un
anello a cinque atomi con due atomi di azoto blu)
disposte una sopra e l'altra sotto il ferro.
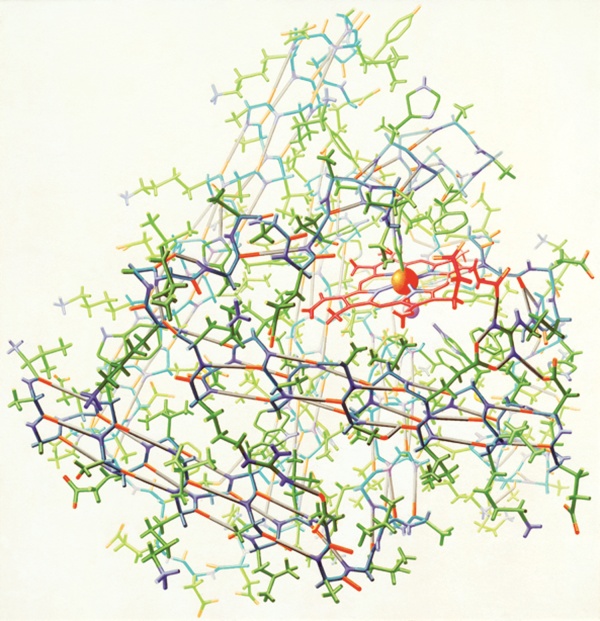 Rappresentare
le strutture Rappresentare
le strutture
Quando è stata risolta la struttura della mioglobina, agli scienziati
si è posto un problema molto complesso. La struttura era così
grande che hanno dovuto inventare nuovi metodi per rappresentarla in
modo soddisfacente. John Kendrew ha costruito un grande modello di fil
di ferro della mioglobina basandosi sui dati sperimentali di densità
elettronica. Poi è stato dato l'incarico ad un artista, Irving
Geis, di realizzare un'immagine della mioglobina. Egli ha realizzato
l'immagine mostrata qui a destra che è stata usata per illustrare
un articolo su Scientific American. La grafica 3D computerizzata sarebbe
stata inventata solo molti anni dopo, quindi egli ha dovuto creare questa
immagine completamente a mano.
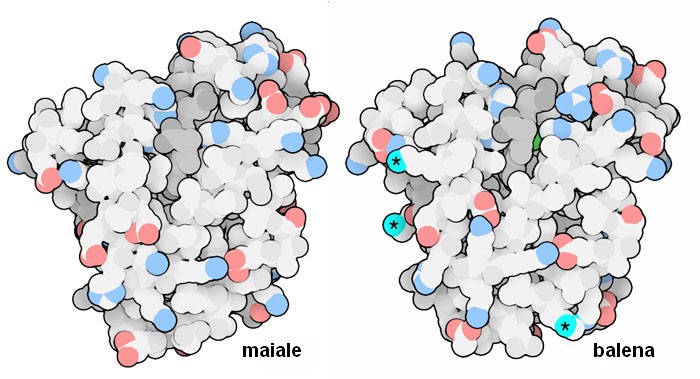 Mioglobina
e balene Mioglobina
e balene
La mioglobina di John Kendrew (file PDB 1mbn) è stata ottenuta dai muscoli spermatici
di balena. Balene e delfini hanno un grande bisogno di mioglobina per
poter immagazzinare più ossigeno per le loro profonde immersioni
sottomarine. Le balene hanno una quantità di mioglobina
circa 30 volte maggiore degli animali terrestri. Uno studio recente
ha rivelato che per accumulare tutta questa mioglobina hanno dovuto
modificarne leggermente la struttura. Confrontando la mioglobina di
maiale (file PDB 1pmb) con quella di
balena (file PDB 1mbn) si nota che sulla
seconda ci sono state alcune mutazioni che hanno introdotto amminoacidi
carichi positivamente sulla superficie (evidenziati nella figura con
un asterisco). Gli animali marini hanno bisogno di queste cariche positive
in più sulla superficie della loro mioglobina per creare forze
repulsive tra le molecole vicine ed impedire così che
la grande concentrazione di mioglobina ne causi l'aggregazione.
Ossigeno legato alla mioglobina
La
struttura originale della mioglobina determinata da John Kendrew, al
posto dell'ossigeno biatomico O2
legato al ferro, ha una molecola di acqua visibile come una sfera rossa
sopra il ferro dell'eme nell'immagine iniziale.
Qui sotto è mostrata
una struttura più recente di mioglobina (file PDB 1mbo)
che contiene invece ossigeno O2
(rosso).
Confrontate le due figure.
Nella prima figura, la catena proteica della mioglobina è rappresentata
con un nastro, e quindi si può vedere facilmente l'ossigeno O2
(rosso) legato all'atomo di ferro (arancione) al centro del gruppo eme.
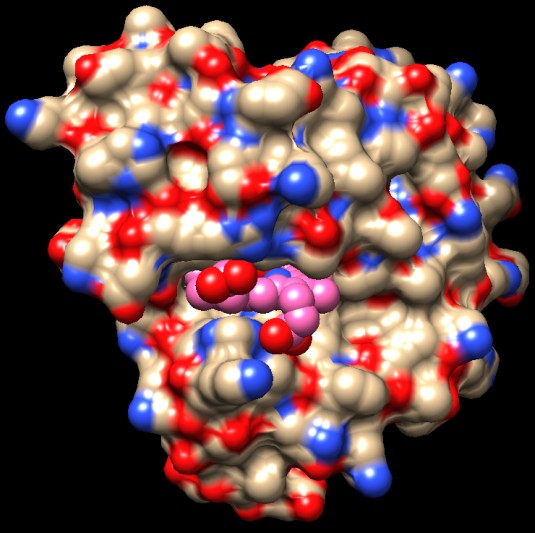
Ma quando, come nella seconda figura, sono rappresentati anche tutti
gli atomi della proteina, l'ossigeno scompare, nascosto all'interno
della tasca.
Come può l'ossigeno entrare e uscire, se è totalmente
circondato dalla proteina? In realtà, la mioglobina (come tutte
le molecole) non è mai ferma, ma compie piccoli movimenti di
espansione, contrazione e torsione. Aperture provvisorie appaiono e
scompaiono in continuazione e permettono all'ossigeno di entrare e uscire.
La struttura mostrata qui è soltanto un'immagine istantanea della
proteina, realizzata quando questa è nella forma ermeticamente
chiusa. La vera struttura della proteina, invece, è dinamica,
ma questi movimenti li possiamo solo immaginare.
Esplorando la struttura
La struttura atomica della mioglobina ha rivelato molti dei principi
base che regolano la struttura e la stabilità delle proteine.
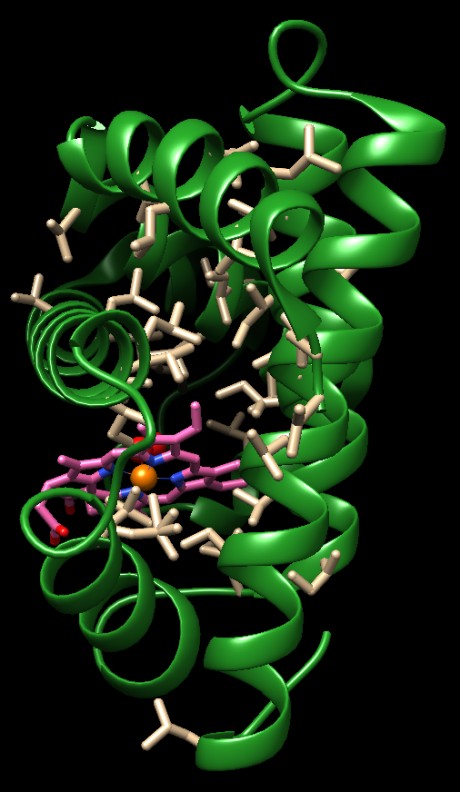
Per esempio si è visto che quando la proteina si ripiega per
assumere la struttura globulare, gli amminoacidi con catene idrocarburiche
apolari si nascondono all'interno della struttura allontanandosi
dall'acqua (immagine qui sotto a sinistra).
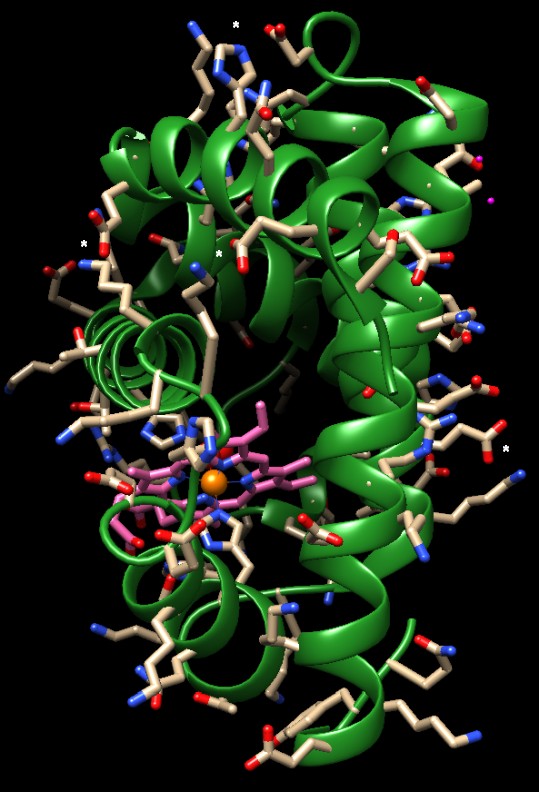
Invece gli amminoacidi con catene laterali polari o cariche elettricamente
sono quasi sempre in superficie rivolti verso l'anbiente acquoso
esterno (immagine qui sotto a destra).
Talvolta formano ponti salini tra gruppi con carica opposta acidi
e basici come i quattro evidenziati in figura con asterischi tra una
lisina e un acido glutammico.
E' anche interessante osservare più da vicino
la struttura del gruppo eme. E' composto da quattro anelli pirrolici
uniti tra loro, ognuno con l'atomo di azoto blu rivolto verso il ferro
al centro. Sopra e sotto vi sono due amminoacidi di istidina che con
il loro anello, che contiene due atomi di azoto blu, si avvicinano molto
al ferro dell'eme. L'istidina superiore (distale, la più distante)
lascia appena lo spazio per la molecola di ossigeno O2
che si lega obliquamente sul ferro. Per confronto si vedano le molecole
del mese emoglobina
(mdm 5/2003) e emoglobina
s-nitrosilata (mdm 5/2019).
. 
Spunti per ulteriori esplorazioni
Usate lo strumento "sequence comparison" per allineare le
sequenze di mioglobine diverse, per individuare eventuali mutazioni.
per esempio, qui trovate l'allineamento
delle mioglobine di balena e maiale che sono state usate per questo
articolo.
La struttura PDB 2jho include una mioglobina
avvelenata con cianuro. Troverete che il cianuro blocca il normale sito
di legame per l'ossigeno.
 Bibliografia Bibliografia
1mbn: J. C. Kendrew, R. E. Dickerson, B. E. Strandberg, R. G. Hart,
D. R. Davies, D. C. Phillips & V. C. Shore (1960) Structure of Myoglobin.
Nature 185, 422-427.
J. C. Kendrew (1961) The three-dimensional structure of a protein molecule.
Scientific American 205(6), 96-110.
1mbo: S. E. Phillips (1980) Structure and refinement of oxymyoglobin
at 1.6 A resolution. Journal of Molecular Biology 142, 531-554.
1pmb: S. J. Smerdon, T. J. Oldfield, E. J. Dodson, G. G. Dodson, R.
E. Hubbard & A. J. Wilkinson (1990) Determination of the crystal
structure of recombinant pig myoglobin by molecular replacement and
its refinement. Acta Crystallographica B, 46, 370-377.
S. Mirceta, A. V. Signore, J. M. Burns, A. R. Cossins, K. L. Campbell
& M. Berenbrink (2013) Evolution of mammalian diving capacity traced
by myoglobin net surface charge. Science 340, 1234192.
|
|
|

 La
prima proteina
La
prima proteina






