|
 2^
Esercitazione Chime 2^
Esercitazione Chime
 Chimica al Computer
Chimica al Computer
 Molecola del Mese
Molecola del Mese
 PianetaChimica home
PianetaChimica home
|
|
Per seguire questa esercitazione dovete naturalmente avere già
scaricato il programma MDL Chime 2.6 al seguente indirizzo:
http://www.mdli.com/chime/
e dovete averlo già installato sul vostro computer.
Chime offre varie opzioni per rappresentare la molecola in molti modi
diversi e questo permette di apprezzarne la struttura sia a livello
complessivo che a livello dei singoli atomi.
Per imparare ad utilizzare Chime provate a seguire questo semplice esercizio.
Mioglobina
In questa esercitazione studierete la mioglobina, una proteina globulare
che si trova nei muscoli e che fissa l'ossigeno O2
utilizzando un gruppo eme.
Per cominciare, scaricate il file della mioglobina 1mbo.zip,
decomprimetelo per ottenere il file PDB 1mbo.pdb e collocatelo
in una directory che chiamerete Mioglobina.
Fate click destro su 1mbo.pdb e nel menù che compare
scegliete Apri con / Internet Explorer. Nella finestra con fondo
nero del browser vedrete la struttura 3D della mioglobina rappresenteta
con tratti sottili (rappresentazione wireframe, fil di ferro). Ora ridimensionate
la finestra di Internet Explorer perchè occupi solo la metà
inferiore dello schermo. Nella metà superiore adattate questa
finestra che contiene la procedura da seguire passo passo.
Esaminare la proteina
1) Trascinate il mouse premendo
il pulsante sinistro per ruotare la mioglobina
2) Premendo shift + pulsante sinistro potete
ingrandirla o rimpicciolirla
3) Premendo shift + pulsante destro potete
ruotarla attorno all'asse perpendicolare allo schermo
4) Premendo Ctrl + pulsante destro potete trascinarla
sullo schermo
5) Premendo pulsante destro compare il menù
principale. Scegliete Display e poi provate tutte le opzioni:
Sticks, Ball and Stick, Spacefill - Van der Waals. Per eliminare
dalla vista le molecole di acqua che appaiono come palline rosse, scegliete
Select - Hetero - Water, poi Select - Hide - Hide selected.
Provate anche le opzioni di display sottostanti che sono attive solo
con proteine, DNA ed RNA.
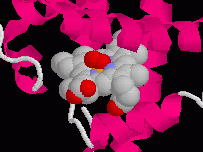
6) Dopo avere scelto l'opzione Cartoons, scegliete
Color - Structure. Vedrete le sei zone ad alfa elica della mioglobina
colorate di porpora (fig. 1), se ci fossero porzioni beta pieghe
sarebbero gialle.
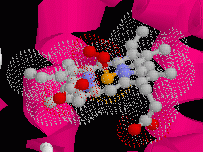
7) Scegliete ora Select - Hetero
- Ligand e poi Display - Spacefill - Van der Waals. Vedrete
il "ligand" cioè l'eme comparire rappresentato con
grosse sfere bianche. Ora scegliete Color - CPK e vedrete ogni
atomo dell'eme assumere un colore convenzionale: C (grigio), N (blu),
O (rosso), Fe (giallo), ecc. L'ossigeno O2
trasportato dalla mioglobina è legato al ferro nel centro dell'eme
ed è visibile come due sfere rosse (fig. 2).
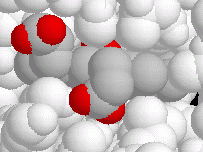
8) Il gruppo eme può anche essere apprezzato così:
scegliete Select - Hetero - Ligand e poi Display - Ball &
Stick, poi scegliete Option - Dot surface - Van der Waals.
Vedrete un'immagine suggestiva degli atomi dell'eme e dello spazio che
occupano (fig. 3).
9) Scegliete ora Select - Residue - HIS e poi Display
- Sticks. Vedrete comparire i residui (amminoacidi) di istidina
HIS. Scegliete Color - Structure e vedrete due istidine color
porpora, proprio vicine al ferro dell'eme, una sopra e una sotto il
piano. Sono le istidine vicinale e distale, che difendono il ferro dai
veleni più insidiosi: il monossido di carbonio e il cianuro.
Osservate come i due atomi di ossigeno di O2
sono legati obliquamente sull'eme e non interferiscono con la struttura
della istidina vicinale (fig. 4).
Prima di continuare, deselezionate Option - Dot surface - Van der
Waals, poi scegliete Select - Select all, poi ancora Display
- Wireframe, siete tornati alle condizioni iniziali.
10) Scegliete ora Select - Protein - Protein e poi
Display - Spacefill - Van der Waals e poi Color - Monochrome.
La proteina appare ora come una massa compatta bianca. Notate che presenta
una cavità. Scegliete ora Select - Hetero - Ligand, e
poi Display - Ball & Stick, e poi Color - CPK. L'eme
diventa visibile incastrato all'interno della proteina (fig. 5).
11) Scegliete infine Display - Spacefill - Van der Waals.
Ruotate e ingrandite la proteina per apprezzare meglio come sia stretto
la spazio disponibile per l'ingresso e l'uscita dell'ossigeno dalla
molecola (fig. 6). La mioglobina reale, però, non è
ferma e rigida come appare in questo modello, ma si espande e si contrae
come una spugna a causa dell'agitazione termica degli atomi che la compongono.
L'ossigeno molecolare può quindi entrare, raggiungere il ferro
dell'eme e poi uscire dalla proteina con relativa facilità.
|