|
|
Proteine e biominerali |
|||||
|
Molecola del mese di aprile 2019 Piccoli cristalli di biominerali vengono usati per costruire ossa, gusci d'uovo e anche minuscole bussole 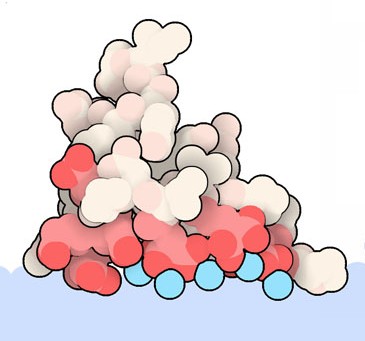 Introduzione IntroduzionePuò sembrare strano, ma due materiali molto diversi come lo smalto dei denti, il materiale più forte del nostro corpo, e il guscio d'uovo, che deve essere abbastanza fragile da consentire ai pulcini di romperlo, sono fatti entrambi al 95% di cristalli minerali. Le differenti caratteristiche di questi due biominerali dipendono dalle proteine che ne hanno costruito i cristalli e da quelle che li hanno assemblati. Proteine biomineralizzanti costruiscono i compartimenti cellulari nei quali vengono fatti crescere i minerali, trasportano ioni in questi compartimenti, innescano la crescita di nuovi cristalli e controllano il rapporto di ioni nei cristalli in crescita. Le proteine possono anche stabilizzare forme cristalline insolite che altrimenti sarebbero instabili. La struttura meravigliosa delle ossa L'osteocalcina mostrata qui a fianco (file PDB 1q8h) è la seconda proteina più abbondante nelle ossa dopo il collagene (osseina) (mdm 4-2000) e agisce anche come un ormone nel promuovere la crescita delle ossa. Nelle ossa si lega alla superficie dei cristalli di idrossiapatite, un minerale composto di calcio e fosfato. La struttura della osteocalcina ci rivela come fa a legarsi alla superficie dei minerali inorganici: su un lato ha un insieme di amminoacidi carichi negativamente (rossi) spaziati alla giusta distanza per riconoscere gli ioni calcio positivi nel cristallo. Nella struttura qui a lato, legati agli amminoacidi negativi in basso, si vedono cinque ioni calcio Ca2+ (azzurri) che sono spaziati tra di loro esattamente come gli ioni nel minerale. Qui sotto sulla sinistra vi è un'altra immagine dell'osteocalcina che mette in evidenza gli amminoacidi carichi negativamente: tre di questi sono acidi glutammici modificati e trasformati in acidi gamma carbossi glutammici (grigi e rossi) che hanno due carbossili ciascuno. Una struttura simile si trova nei fattori della coagulazione che si legano ai fattori di tessuto (mdm 3-2006). 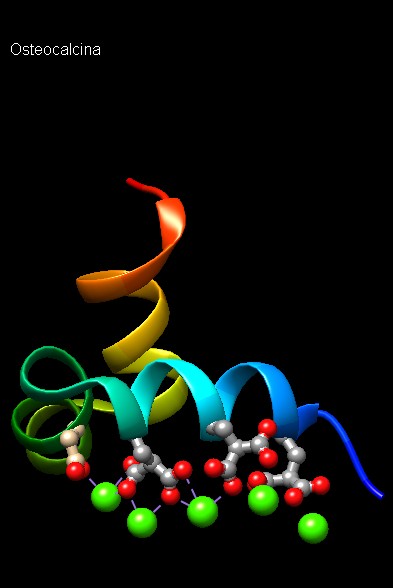 . .
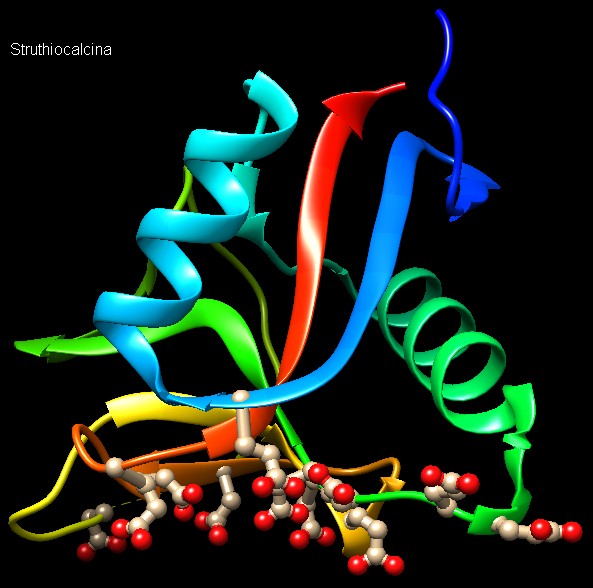
Gusci d'uovo I gusci d'uovo contengono calcite, un minerale di carbonato di calcio impaccato in una matrice di proteine. Come l'osteocalcina, la proteina del guscio d'uovo struthiocalcina (o struzzocalcina) mostrata qui sopra sulla destra (file PDB 4uww) si lega alla superficie del cristallo di minerale usando una matrice di amminoacidi negativi (acidi aspartico e glutammico, beige e rossi) che si legano agli ioni calcio positivi (non mostrati) e guidano la crescita dei cristalli durante la costruzione del guscio. Studi compiuti su uova di struzzo fossili hanno dimostrato che questa interazione proteina-minerale è così forte che frammenti di questi complessi possono resistere anche per milioni di anni. Il tipo di avvolgimento della struthiocalcina (detto lectina di tipo C) è simile a quello delle proteine antigelo che si legano alla superficie dei cristalli di ghiaccio (mdm 12-2009) e si pensa che si siano evolute da un antenato comune. Costruire minerali Usando come modelli le proteine biomineralizzanti naturali, gli scienziati stanno progettando piccoli peptidi per guidare la sintesi di minerali in laboratorio. Questi peptidi sono costituiti da semplici strutture ad alfa elica o beta pieghe che contengono sequenze ripetute di amminoacidi acidi per riprodurre la superficie che si lega ai minerali della struthiocalcina. Finora i ricercatori hanno ingegnerizzato con successo peptidi in grado di formare vaterite, un minerale di carbonato di calcio diverso dalla calcite del guscio d'uovo. Minerali magnetici Sorprendentemente, i batteri, gli uccelli e altri organismi sanno costruire piccoli cristalli di magnetite, che funzionano come bussole, per sentire il campo magnetico terrestre. Gli uccelli ne hanno bisogno per orientarsi durante le loro migrazioni che attraversano i continenti. I batteri anaerobi li usano per orientarsi localmente: il campo magnetico terrestre punta verso i poli, ma anche verso il basso, così questi batteri lo usano per andare verso il basso, lontano dalla superficie dove c'è ossigeno che per loro è un veleno. In questi batteri vi è un organello sensibile al campo magnetico chiamato magnetosoma formato da cristalli di magnetite inclusi in una vescicola lipidica. Qui sotto è mostrato l'enzima batterico magnetocromo (MamP) (file PDB 4jj0) che costruisce i cristalli di magnetite, un ossido di ferro con intense proprietà magnetiche di formula Fe(II)Fe(III)2O4. MamP è una proteina dimera dove ognuna delle due subunità (blu scuro e blu chiaro) è formata da un dominio centrale legato a due domini consecutivi magnetocromici. Il dominio centrale possiede molti amminoacidi di acido glutammico (verdi e rossi) che formano al centro una tasca dove il ferro inizia a formare il cristallo. Dato che nella magnetite gli ioni ferro che si legano all'ossigeno devono essere Fe2+ e Fe3+ in rapporto 1:2, nei domini magnetocromici vi sono gruppi eme (rosa, simili a quelli del citocromo c) che estraggono un elettrone da alcuni ioni Fe2+ per generare la giusta quantità di ioni Fe3+ nel cristallo di magnetite in crescita. 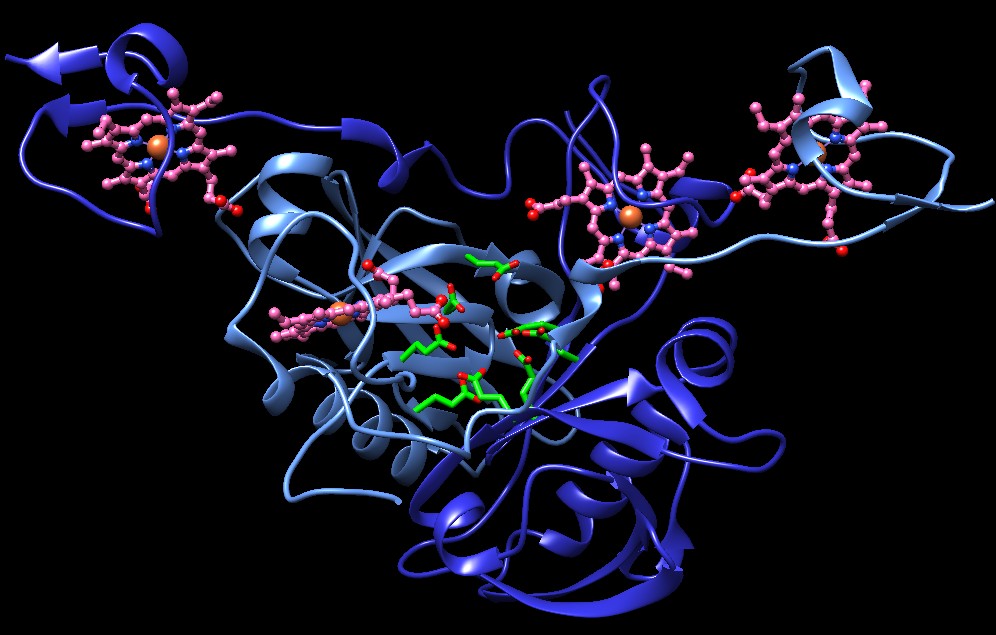 Esplorando la struttura Gli scienziati stanno imitando il processo di biomineralizzazione come strategia per la produzione di particolari nanocristalli da usare in materiali ingegnerizzati con particolari proprietà magnetiche, ottiche o mediche. Qui sotto, per esempio, è mostrata la proteina artificiale nvPizza2-S16H58 (file PDB 5chb) che racchiude a sandwich il più piccolo nanocristallo conosciuto, una perfetta struttura 3D formata da 7 ioni cadmio (viola) e 12 ioni cloro (verdi). In questa proteina artificiale, il nanocristallo cadmio-cloruro è coordinato da un insieme di istidine (rosa) disposte in modo simmetrico che si estendono verso l'interno del complesso proteico e interagiscono con gli ioni cadmio. La proteina è formata da due subunità uguali che hanno una notevole struttura ad elica a sei pale e sono formate da tre catene costituite da tratti beta pieghe (gialli). Due ioni solfato (sfere gialle e rosse) occupano lo spazio interno all'elica sia sopra che sotto. . . . . . . . . . . .. . . . . . 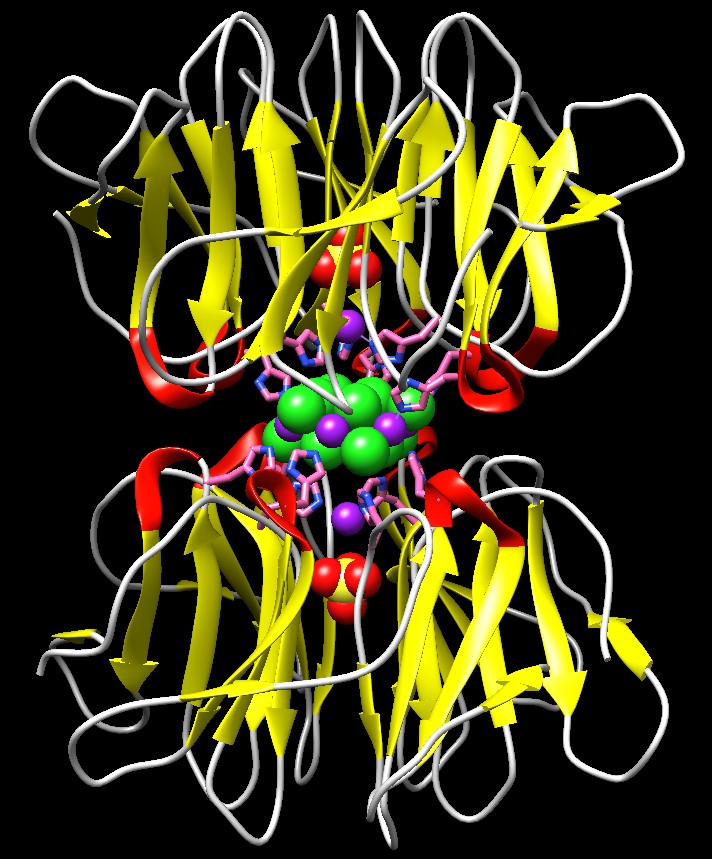 La struttura dell'elica a sei pale beta pieghe è mostrata qui sotto vista di fronte. . . . . . . . . . . . . . . . . . . 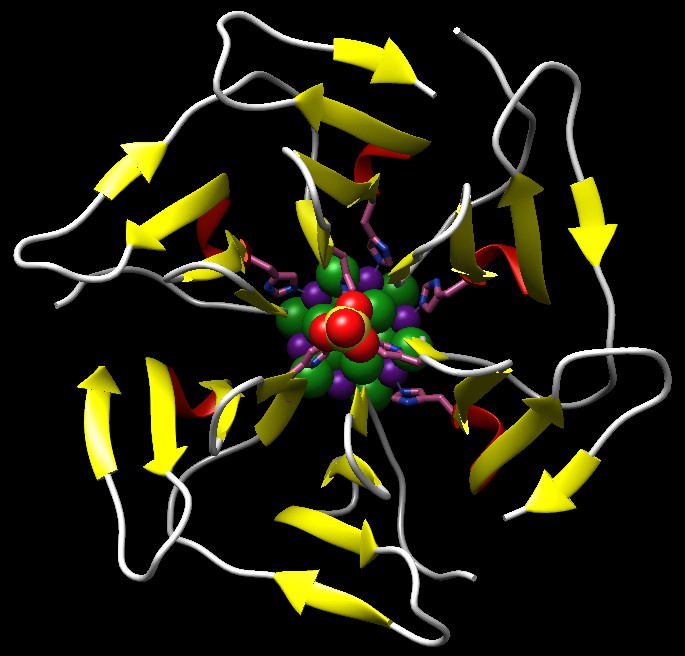
Spunti per ulteriori esplorazioni Nella formazione dei cristalli di magnetite sono coinvolte molte altre proteine. Per esaminarle, cercate per "magnetite" nel sito RCSB PDB. Usate l'opzione "Structure Alignment View" per confrontare strutture simili alla struthiocalcina e ad altre proteine antigelo. Lu, H., Lutz, H., Roeters, S.J., Hood, M.A., Schäfer, A., Muñoz-Espí, R., Berger, R., Bonn, M., Weidner, T. (2018) Calcium-Induced molecular rearrangement of peptide folds enables biomineralization of vaterite calcium carbonate. Journal of the American Chemical Society 140: 2793-2796. Demarchi, B., Hall,S., Roncal-Herrero, T., Freeman, C.L., Woolley, J., Crisp, M.K., Wilson, J., Fotakis, A., Fischer, R., Kessler, B.M., Rakownikow, R., Jersie-Christensen, J.V., Olsen, J., Haile, J., Thomas, C.W., Marean, J., Parkington, S., Presslee, J., Lee-Thorp, P., Ditchfield, J.F., Hamilton, M.W., Ward, C.M., Wang, M.D., Shaw, T., Harrison, M., Domínguez-Rodrigo, R., MacPhee, A., Kwekason, M., Ecker, L., Kolska Horwitz, M., Chazan, R., Kröger, J., Thomas-Oates, J.H., Harding, E., Cappellini, K., Penkman Collins, M.J. (2016) Protein sequences bound to mineral surfaces persist into deep time. Elife 5: e17092. 4uww: Ruiz-Arellano, R.R., Medrano, F.J., Moreno, A., Romero, A. (2015) Structure of struthiocalcin-1, an intramineral protein from Struthio camelus eggshell, in two crystal forms. Acta Crystallographica D Biological Crystallography 71: 809-818. 5chb: Voet, A.R., Noguchi, H., Addy, C., Zhang, K.Y., Tame, J.R. (2015) Biomineralization of a Cadmium Chloride Nanocrystal by a Designed Symmetrical Protein. Angewandte Chemie International Edition English 54: 9857-9860. 4jj0: Siponen, M.I., Legrand, P., Widdrat, M., Jones, S.R., Zhang, W.J., Chang, M.C., Faivre, D., Arnoux, P., Pignol, D. (2013) Structural insight into magnetochrome-mediated magnetite biomineralization. Nature 502: 681-684. 2zib: Nishimiya, Y., Kondo, H., Takamichi, M., Sugimoto, H., Suzuki, M., Miura, A., Tsuda, S. (2008) Crystal structure and mutational analysis of Ca2+-independent type II antifreeze protein from longsnout poacher, Brachyopsis rostratus. Journal Molecular Biology 382: 734-746. 1q8h: Hoang, Q.Q., Sicheri, F., Howard, A.J., Yang, D.S. (2003) Bone recognition mechanism of porcine osteocalcin from crystal structure. Nature 425: 977-980. Blakemore, R.P., Frankel, R.B., Kalmijn, A.J. (1980) South-seeking magnetotactic bacteria in the Southern Hemisphere. Nature 286: 384-385.
|
||||||
|
|
||||||
