|
|
Proteine e nanoparticelle |
||||||
|
Molecola del Mese di Giugno 2018 I ricercatori di nanotecnologia stanno progettando nuovi metodi per combinare proteine e nanoparticelle  Introduzione IntroduzioneIn natura il carbonio puro si può trovare in tre forme forme allotropiche, diamante, grafite e fullerene. Nel diamante gli atomi di carbonio formano una struttura tridimensionale tetraedrica che lega insieme con legami covalenti miliardi di atomi e dona al diamante la sua straordinaria forza. Nella grafite gli atomi di carbonio formano dei fogli bidimensionali forti in sè, ma legati debolmente gli uni agli altri e questo conferisce al materiale morbidezza e scivolosità. Nel 1985, i ricercatori hanno scoperto una nuova forma di carbonio con 60 atomi legati insieme per formare una sfera cava. Dato che questa struttura somigliava alle cupole geodetiche disegnate da Buckminster Fuller, la nuova molecola è stata chiamata fullerene e la si può vedere qui sulla destra. Alcuni degli anelli di cui è composta sono esagoni formati da sei atomi di carbonio, altri sono pentagoni. Ogni pentagono è circondato da cinque esagoni. Come il diamante e la grafite, questa nuova forma di carbonio ha delle proprietà ben definite: i fullereni e i nanotubi (una loro variante a forma di tubo) conducono l'elettricità e il calore, ma la cosa straordinaria è che sono formati di singole nanoparticelle simmetriche con proprietà così sorprendenti che sono diventate il soggetto preferito della nanotecnologia. Il difetto principale dei fullereni è che sono insolubili in acqua. I ricercatori stanno studiando nuove interazioni tra proteine e fullereni (e altre nanoparticelle) da applicare in medicina e nanotecnologia. Legare una proteina ai fullereni Per progettare una proteina che si leghi ai nanotubi, i ricercatori hanno osservato che la geometria di un'alfa elica di una proteina si adatta alla geometria a nido d'ape del grafene. Così hanno messo degli amminoacidi di alanina lungo l'alfa elica opportunamente spaziati per incontrare il centro delle unità ripetenti esagonali di un foglio di grafene. Poi hanno progettato una proteina che conteneva un fascio di quattro alfa eliche capaci di affiancarsi al nanotubo e di avvolgerlo. Quando hanno sintetizzato la proteina, hanno scoperto che si legava ai nanotubi proprio come avevano progettato. E inoltre, per puro caso, sono riusciti ad inglobare anche fullereni in un altro punto nella proteina: un amminoacido di tirosina della catena si era girato all'esterno, inaspettatamente, formando una piccola tasca capace di legare un fullerene. Complessi conduttori Questa alfa elica progettata dai ricercatori e chiamata COP (C60-organizing peptide) forma un complesso cristallino quando viene mescolata ai fullereni. Nella figura in alto (file PDB 5et3) si vede che due peptidi COP affiancati (uno azzurro e l'altro blu) abbracciano il fullerene con i loro amminoacidi di tirosina (verde), e formano una grande struttura sopramolecolare con molte COP e fullereni in posizioni definite. Se vengono presi separatamente, i fullereni e le proteine COP non sono conduttori, ma questa struttura ordinata tridimensionale di nanoparticelle e proteine conduce l'elettricità. Calixareni che incapsulano 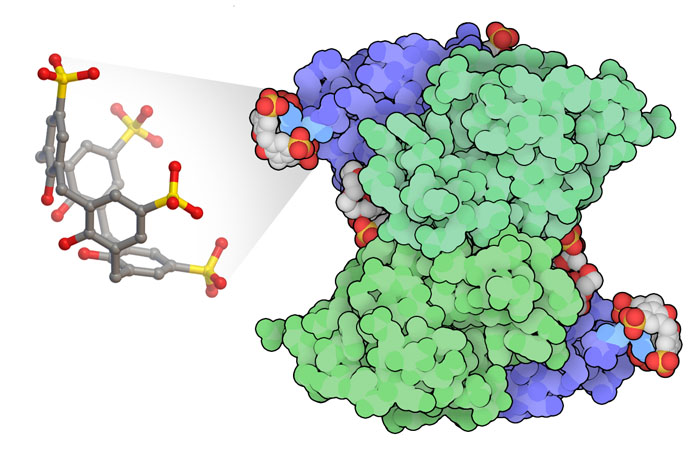 I
ricercatori stanno anche progettando nanoparticelle per svolgere compiti
particolari e stanno cercando di combinarle con proteine. I calixareni,
per esempio, sono formati da quattro anelli benzenici legati da ponti
CH2 per creare una
specie di tubo. Su un lato degli anelli benzenici sono legati dei gruppi
ingombranti solfonici (gialli e rossi) che costringono la struttura ad
aprirsi per formare una specie di coppa. Se progettati correttamente,
con i giusti gruppi chimici legati sul bordo, i calixareni possono legare
selettivamente molecole diverse neutre o cariche. All'inizio erano stati
progettati per legare piccole molecole o ioni, ma in seguito i ricercatori
li hanno modificati per indurli a legarsi alla superficie delle proteine.
La struttura mostrata qui a destra è quella del lisozima
(mdm 9-2000) con alcuni calixareni legati alla sua superficie (file PDB
4prq). In questa struttura i calixareni
stanno facendo due cose diverse. Alcuni riconoscono e mascherano la carica
positiva di un amminoacido di arginina sulla superficie del lisozima,
mentre altri legano le molecole di PEG (polietilenglicole usato
per far cristallizzare la proteina) e agiscono come dei grumi di colla
che riempiono gli spazi tra le proteine. Con queste interazioni i calixareni
favoriscono l'aggregazione del lisozima per formare tetrameri che poi
si combinano ulteriormente per formare lunghe catene. Gli scienziati stanno
esaminando altre molecole leganti come i calixareni per promuovere o inibire
l'aggregazione proteica per migliorare le tecniche di cristallizzazione
delle proteine. I
ricercatori stanno anche progettando nanoparticelle per svolgere compiti
particolari e stanno cercando di combinarle con proteine. I calixareni,
per esempio, sono formati da quattro anelli benzenici legati da ponti
CH2 per creare una
specie di tubo. Su un lato degli anelli benzenici sono legati dei gruppi
ingombranti solfonici (gialli e rossi) che costringono la struttura ad
aprirsi per formare una specie di coppa. Se progettati correttamente,
con i giusti gruppi chimici legati sul bordo, i calixareni possono legare
selettivamente molecole diverse neutre o cariche. All'inizio erano stati
progettati per legare piccole molecole o ioni, ma in seguito i ricercatori
li hanno modificati per indurli a legarsi alla superficie delle proteine.
La struttura mostrata qui a destra è quella del lisozima
(mdm 9-2000) con alcuni calixareni legati alla sua superficie (file PDB
4prq). In questa struttura i calixareni
stanno facendo due cose diverse. Alcuni riconoscono e mascherano la carica
positiva di un amminoacido di arginina sulla superficie del lisozima,
mentre altri legano le molecole di PEG (polietilenglicole usato
per far cristallizzare la proteina) e agiscono come dei grumi di colla
che riempiono gli spazi tra le proteine. Con queste interazioni i calixareni
favoriscono l'aggregazione del lisozima per formare tetrameri che poi
si combinano ulteriormente per formare lunghe catene. Gli scienziati stanno
esaminando altre molecole leganti come i calixareni per promuovere o inibire
l'aggregazione proteica per migliorare le tecniche di cristallizzazione
delle proteine.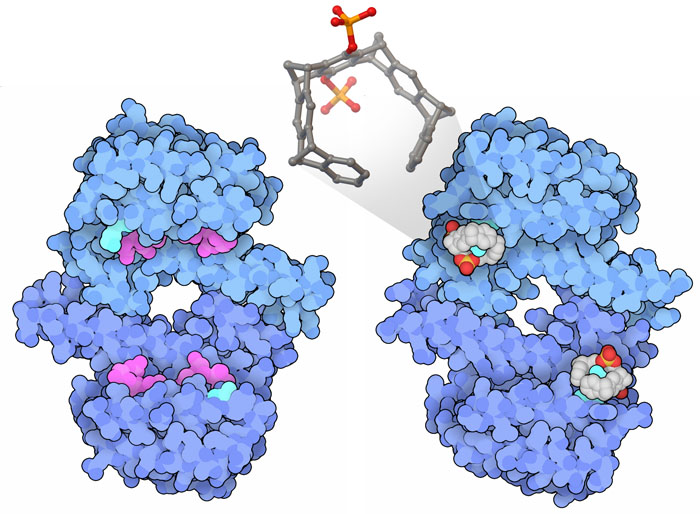 Modulatori
proteici Modulatori
proteiciI ricercatori stanno anche progettando nanoparticelle che si leghino a specifici amminoacidi per modulare la funzione della proteina. Per esempio, è stata progettata una pinza molecolare a forma di C, a cui sono legati due gruppi fosfato negativi, che la rendono sia solubile in acqua che capace di legarsi in modo specifico ad amminoacidi con carica positiva come lisina e arginina. I ricercatori hanno scoperto che questa nanoparticella inibisce la segnalazione della proteina 14-3-3. Nella struttura (file PDB 5oeh), la pinza si lega ad una singola arginina che sporge dalla superficie. Come si vede nella struttura PDB 3nkx, questa lisina si trova vicino al sito dove si legano piccoli peptidi di segnalazione (come C-RAF magenta), suggerendo che la pinza agisca bloccando il legame o ostacolando l'ingresso dei peptidi di segnalazione. 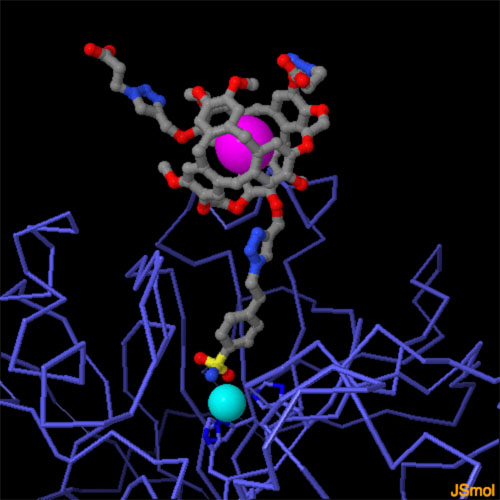 Esplorando
la struttura Esplorando
la strutturaUn isotopo dello xenon (Xe 129) è usato nella diagnostica medica come mezzo di contrasto negli esami di risonanza magnetica. Lo si usa sia come gas per evidenziare le cavità del fegato, sia sciolto nei liquidi corporei per mettere in evidenza il flusso sanguigno e i tessuti. Sono stati progettati specifici criptofani per portare lo Xenon a specifiche proteine. I criptofani sono dei gusci vuoti che hanno ai lati delle aperture che consentono l'ingresso di molecole ospiti. Il criptofano mostrato qui ha le dimensioni esatte per ospitare un singolo atomo di xenon (magenta) ed è legato ad uno specifico inibitore della anidrasi carbonica che sa legarsi ad un atomo di zinco (ciano) nel sito attivo dell'enzima come si vede nelle figura qui a fianco (file PDB 3cyu). Dopo che il criptofano contenente lo xenon si è legato alla proteina bersaglio, la risonanza magnetica rileva la posizione nel corpo degli atomi di xenon (e quindi della proteina bersaglio). Spunti per ulteriori approfondimenti Il riconoscimento di molecole bersaglio da parte di una proteina può avvenire anche con amminoacidi non carichi. Per esempio, provate a cercare agli amminoacidi dell'insulina riconosciuti dalla parte interna del cucurbituril, una molecola che ha la forma di una zucca (file PDB 3q6e, esaminate la seconda struttura biologica che include la nanoparticella). Per esaminare la struttura delle nanoparticelle cercate fullerene e " molecular tweezer "nel Ligand Depot.  Bibliografia BibliografiaS van Dun, C Ottmann, LG Milroy & L Brunsveld (2017) Supramolecular chemistry targeting proteins. Journal of the American Chemical Society 139, 13960-13968. 5et3: KH Kim, DK Ko, YT Kim, NH Kim, J Paul, SQ Zhang, CB Murray, R Acharya, WF DeGrado, YH Kim & G Grigoryan (2016) Protein-directed self-assembly of a fullerene crystal. Nature Communications 7, 11429-11429. 4prq: RE McGovern, AA McCarthy & PB Crowley (2014) Protein assembly mediated by sulfonatocalix[4]arene. Chemical Communications 50, 10412-10415. 5oeh: D Bier, R Rose, K Bravo-Rodriguez, M Bartel, JM Ramirez-Anguita, S Dutt, C Wilch, FG Klärner, E Sanchez-Garcia, T Schrader & C Ottmann (2013) Molecular tweezers modulate 14-3-3 protein-protein interactions. Nature Chemistry 5, 234-239. 3nkx: M Molzan, B Schumacher, C Ottmann, A Baljuls, L Polzien, M Weyand, P Thiel, R Rose, M Rose, P Kuhenne, M Kaiser, UR Rapp, J Kuhlmann & C Ottmann (2010) Impaired binding of 14-3-3 to C-RAF in Noonan syndrome suggests new approaches in diseases with increased Ras signaling. Molecular Cell Biology 30, 4698-4711. 3q6e: JM Chinai, AB Taylor, LM Ryno, ND Hargreaves, CA Morris, PJ Hart & AR Urbach (2011) Molecular recognition of insulin by a synthetic receptor. Journal of the American Chemical Society 133, 8810-8813. G Grigoryan, YH Kim, R Acharya, K Axelrod, RM Jain, L Willis, M Drndic, JM Kikkawa & WF DeGrado (2011) Computational design of virus-like protein assemblies on carbon nanotube surfaces. Science 332, 1071-1076. 3cyu: JA Aaron, JM Chambers, KM Jude, L Di Costanzo, IJ Dmochowski & DW Christianson (2008) Structure of a 129Xe-cryptophane biosensor complexed with human carbonic anhydrase II. Journal of the American Chemical Society 130, 6942-6943. MM Spence, SM Rubin, IE Dimitrov, EJ Ruiz, DE Wemmer, A Pines, SQ Yao, F Tian & PG Schultz (2001) Functionalized xenon as a biosensor. Proceedings of the National Academy of Science USA 98, 10654-10657. J Baggott (1996) Perfect symmetry - The accidental discovery of buckminsterfullerene. Oxford University Press.
|
|||||||
|
|
|||||||
