|
|
Proteasi romboide |
|||||
|
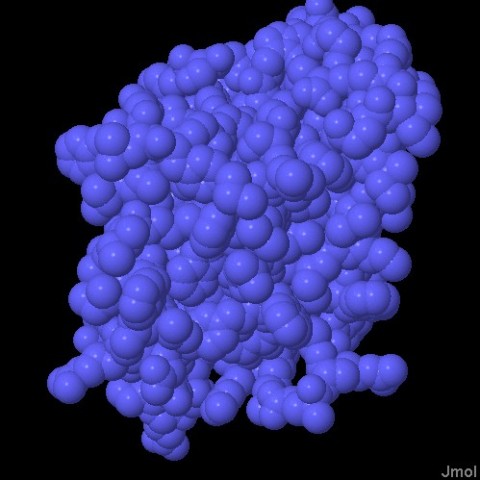
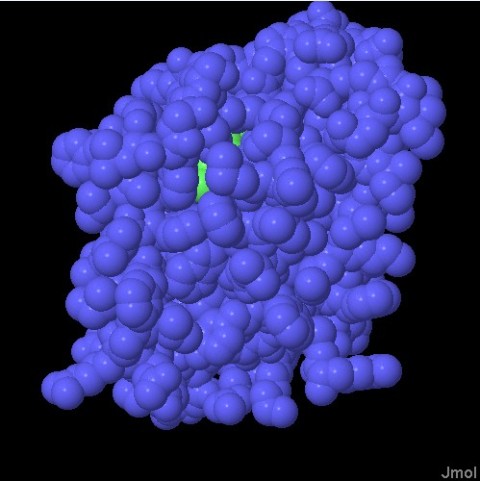
Molecola del Mese di Agoso 2011 Alcune proteasi intermembrana, dette romboidi, tagliano le proteine immerse nella membrana cellulare 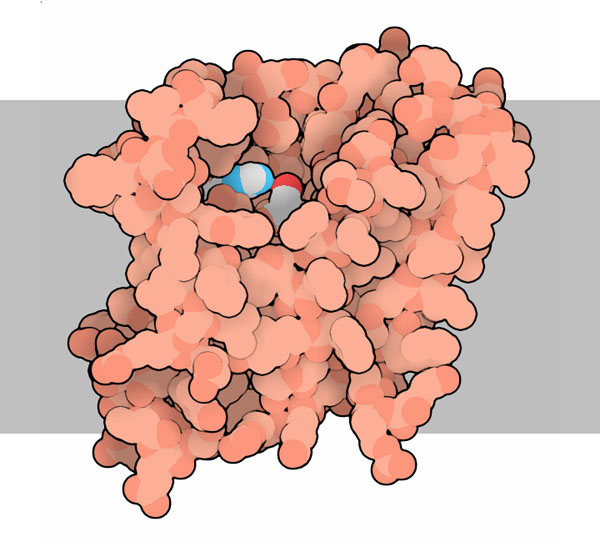 Introduzione IntroduzioneLe proteasi sono enzimi che tagliano le catene proteiche e possono avere forme e dimensioni molto diverse. Le proteasi più note sono probabilmente pepsina (mdm 12-2000) e tripsina (mdm 10-2003), vere e proprie macchine di distruzione che hanno il compito di digerire le proteine che introduciamo con la dieta. La maggior parte delle proteasi nelle nostre cellule, però, vengono utilizzate per scopi molto più delicati, regolano l'azione di altre proteine operando dei tagli specifici nelle loro catene. In alcuni casi questi tagli possono attivare le proteine, in altri casi le distruggono definitivamente. In entrambi i casi la trasformazione è veloce e permanente, e attiva o disattiva le proteine bersaglio. Proteasi di membrana Per molti anni si è creduto che le proteasi fossero enzimi piccoli e solubili, perchè si conoscevano solo le proteasi della digestione che sono molto abbondanti e facili da studiare. Ora però si sa che le proteasi possono avere forme e dimensioni molto diverse che vanno dai piccoli e stabili enzimi digestivi, ai grandi proteasomi (vedi mdm 12-2004 ubiquitina) che degradano le proteine non più utili nelle cellule. Negli ultimi dieci anni, però, si è scoperta una nuova classe di proteasi, quelle di membrana che tagliano altre proteine di membrana. Proteasi romboide La prima serina proteasi intermembrana è stata scoperta in un moscerino della frutta mutante che veniva chiamato romboide a causa della strana forma della sua testa. Questa proteasi ha preso il nome dal moscerino mutante perchè regola proprio il recettore della crescita che determina la strana forma del moscerino. Stranamente, anche la forma della proteasi, se osservata da una particolare prospettiva, ricorda quella di un rombo immerso nella membrana cellulare. La proteasi mostrata qui sopra è la GlpG, una proteasi romboide batterica (file PDB 2nrf). Si nota la tasca del sito attivo nella forma aperta che possiede sul fondo i due amminoacidi attivi: istidina (bianca e blu) e serina (bianca e rossa). (vedi anche le strutture 2ic8 e 2irv) Componenti del sito attivo I ricercatori hanno scoperto che molti tipi di proteasi intermembrana sfruttano i meccanismi di reazione tipici delle proteasi solubili. Le proteasi romboidi possiedono, nel loro sito attivo, la coppia di amminoacidi serina-istidina, tipica delle serina-proteasi come tripsina e chimotripsina. La famiglia di proteasi sito-2, come la proteasi batterica mostrata qui sotto sulla sinistra (file PDB 3b4r), usa uno ione zinco (in magenta nella figura) come altre metallo-proteasi del tipo della carbossipeptidasi. Infine, all'interno delle membrane, si sono scoperte anche delle proteasi acide come la preflagellina peptidasi FlaK, mostrata qui sotto sulla destra (file PDB 3s0x), e il grande complesso gamma secretasi (non illustrato qui, mdm 7-2009) che ha un ruolo importante nello sviluppo del morbo di Alzheimer. 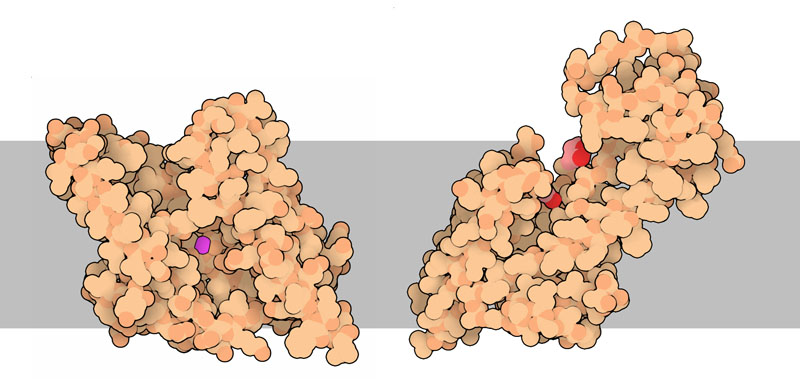 Esplorando la struttura Le proteasi intermembrana svolgono uno strano compito. Per realizzare la loro azione devono essere inserite nel cuore idrofobico della membrana, ma hanno anche bisogno di acqua e di amminoacidi polari che leghino acqua. Per questo posiedono un segmento flessibile che copre il sito attivo e che, spostandosi, consente alla proteina bersaglio e all'acqua di entrare. Le tre strutture mostrate qui sotto rivelano questa flessibilità, anche se la cosa è ancora controversa perchè lo studio delle proteine di membrana è particolarmente difficile e richiede l'uso di tecniche artificiali per stabilizzare le proteine dopo averle estratte dalla membrana. Qui sotto a sinistra è mostrata una struttura perfettamente chiusa (file PDB 2ic8), Al centro si può vedere, invece, un enzima nella forma completamente aperta (file PDB 2nrf). Infine sulla destra è mostrato una enzima che si è chiuso attorno al suo bersaglio (file PDB 2xow). In realtà qui si è usata una molecola che è solo simile al suo normale bersaglio, ma che non può essere tagliata e così si è potuto cristallizzare il complesso intatto. Gli amminoacidi del sito attivo istidina e serina sono evidenziati nelle tre strutture. 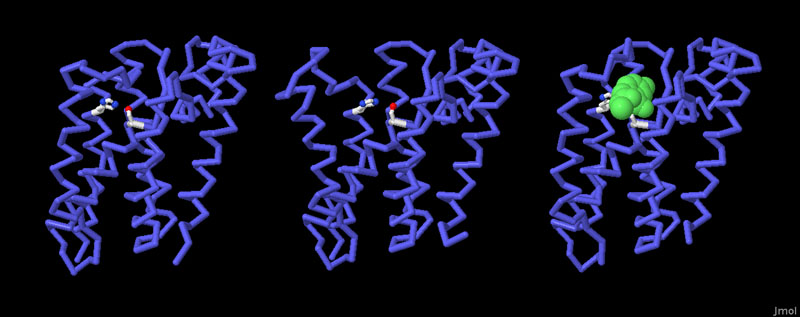 Qui sotto le tre strutture sono riproposte in dettaglio. Nelle immagini di destra, che mostrano il reale ingombro degli atomi, si apprezza meglio quanto chiusa o aperta sia la struttura per l'accesso al sito attivo che contiene i due amminoacidi istidina e serina. 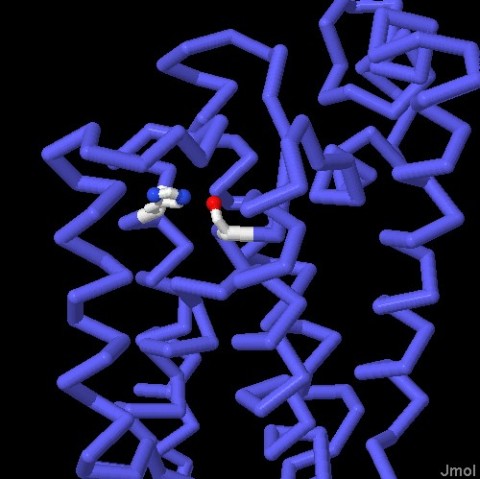 . . .
. . . 
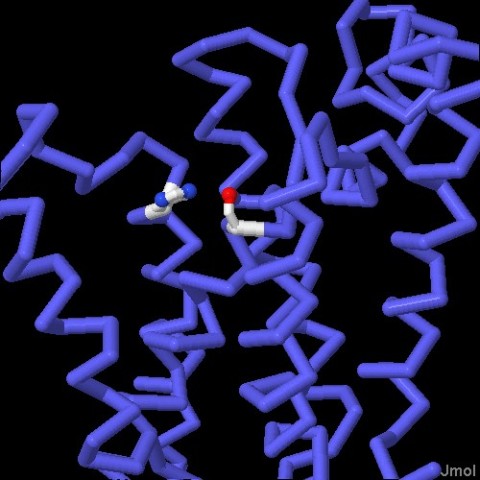 . . .
. . . 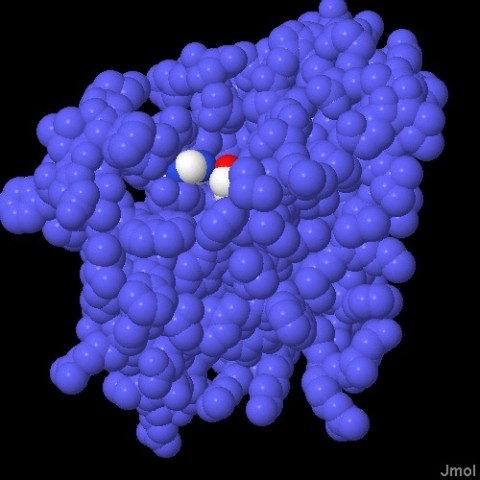 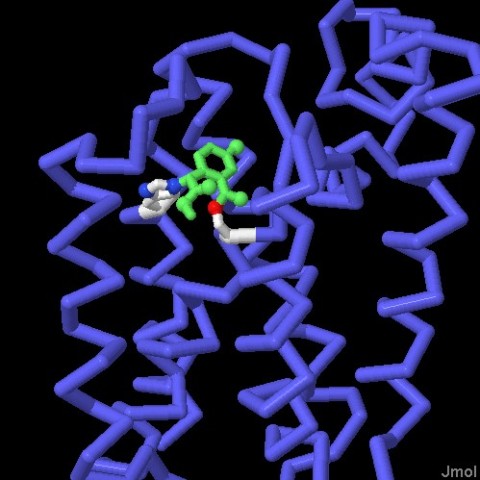 . . .
. . .  Spunti per ulteriori esplorazioni 1. Il file PDB 3b4r contiene due copie della stessa proteina, una è nella forma aperta e l'altra nella forma chiusa. Usate la funzione "Structure Comparison" nel sito PDB per comparare queste due forme, oppure osservate la struttura di queste due proteine lanciando il file PDB 3b4r con Internet Explorer dopo aver installato il plug-in CHIME (vedi chimica al computer) o infine usando programmi come ArgusLab che permettono di esplorare la struttura 3D delle proteine 2. Le proteine di membrana di solito possiedono una fascia di amminoacidi apolari sulla loro superficie nella zona dove sono immerse nella membrana. Potete verificare questo fatto andando nella pagina PDB di una proteasi romboide (o di un'altra proteina di membrana), e scegliere l'opzione "View in Jmol", poi colorate gli amminoacidi in base alla loro polarità. In alternativa usando CHIME scegliete le opzioni: Select - Protein - Hydrophobic e poi colorate la porzione selezionata con un colore di vostra scelta, per esempio: Select - Change Color To - Green.
|
||||||
|
|
||||||
