|
Molecola del Mese di giugno 2010
EGF fa parte di una famiglia di piccole proteine che controllano la crescita
dei tessuti stimolando la divisione cellulare per mitosi
 Introduzione Introduzione
Le nostre cellule comunicano costantemente tra loro per negoziare il trasporto
e l'uso delle risorse e per decidere quando crescere, quando fermarsi,
quando morire. Spesso questi messaggi sono portati da piccole proteine
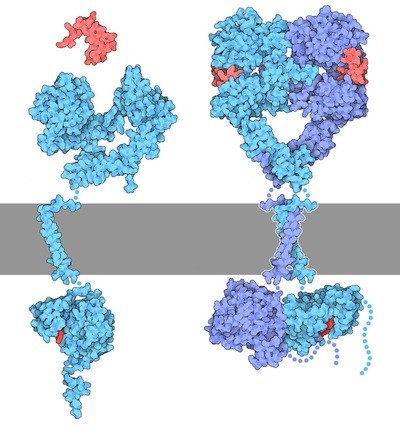
come il fattore di crescita epiteliale EGF mostrato in rosso qui a destra
(file PDB 1egf). Il fattore EGF è
un messaggero che dice alle cellule di crescere. E' rilasciato
dalle cellule che si trovano in un'area di crescita attiva e viene catturato
dalla stessa cellula che l'ha prodotto o dalle sue vicine e ne stimola
la mitosi, cioè la divisione cellulare. Il fattore EGF è
catturato da un recettore EGF sulla superficie cellulare che in seguito
rilascia un messaggio di segnalazione all'interno della cellula, stimolando
alla fine i processi che portano alla divisione cellulare per mitosi e
quindi alla crescita.
Domini e dimeri
Il recettore EGF, mostrato qui in azzurro, è
una proteina flessibile con molte parti mobili che comprende una grande
porzione extracellulare, una porzione che attraversa la membrana, un
dominio con attività di chinasi e una lunga coda flessibile.
La porzione rivolta verso l'esterno della cellula, mostrata in alto
nella figura, è composta di quattro domini flessibili che riconoscono
EGF. Quando questa porzione non sta legando EGF, si ripiega su se stessa
come è mostrato nella figura di sinistra, quando però
si lega a EGF, il recettore si apre e si lega ad una seconda copia dello
stesso recettore formando così il complesso dimero mostrato
sulla destra. Questo fa legare tra loro due copie del dominio chinasi
all'interno della cellula (in basso a destra nella figura). Poichè
i domini chinasi sono vicini uno all'altro, possono fosforilare
alcune tirosine nelle code lunghe e flessibili del recettore (mostrate
qui solo con dei puntini). Le code fosforilate stimolano le proteine
di segnalazione all'interno della cellula.
Sorprese strutturali
Poichè il recettore EGF è così
flessibile, è stato studiato rompendolo in molti frammenti che
sono stati esaminati uno per uno separatamente. Per ricostruire questa
immagine, quindi, sono stati utilizzati molti file PDB 1nql,
1ivo, 2jwa,
1m17 e 2gs6.
Le strutture di queste porzioni del recettore EGF hanno riservato molte
sorprese.
Prima di tutto i ricercatori hanno scoperto che EGF si lega ai due
lati del recettore e non nel centro come in altri recettori di questo
tipo. Sembra che EGF modelli la struttura del recettore fino a fargli
assumere la forma in grado di dimerizzare, invece di comportarsi come
un collante tra le due catene.
Inoltre un'attenta analisi del dominio chinasi ha mostrato che
questo viene attivato da una fusione assimmetrica testa-coda,
nonostante la fusione simmetrica della porzione extracellulare
Una grande famiglia
EGF e il recettore EGF fanno parte di una grande
famiglia di proteine che controllano la crescita e lo sviluppo delle
cellule. In questa famiglia ci sono almeno sette proteine messaggero
simili come il fattore di crescita trasformante alfa e
l'anfiregulina e quattro recettori chiamati collettivamente ErbB
o recettori HER. Questi messaggeri e recettori possono mescolarsi
e accoppiarsi. Messaggeri diversi possono legare insieme due recettori
identici o due recettori diversi. In questo modo il sistema, pur disponendo
di un numero limitato di messaggeri e recettori, può mandare
un molti messaggi diversi per incontrare le esigenze di ogni
tipo di cellula.
 Spegnere
il recettore Spegnere
il recettore
Naturalmente, dopo che il recettore EGF è
stato attivato da un messaggero e ha mandato il segnale all'interno
della cellula, bisogna spegnerlo, altrimenti continuerà a mandare
quel segnale in modo incontrollato. Un enzima apposito realizza questa
operazione staccando i gruppi fosfato che sono stati aggiunti alle code
flessibili del recettore per attivarlo. La proteina tirosina fosfatasi
1B (file PDB 1ptu) è mostrata qui
a destra in arancione con un breve tratto di catena proteica fosforilata
legata nel suo sito attivo. La tirosina fosforilata si trova immersa
in profondità nel sito attivo (in trasparenza è visibile
il suo gruppo fosfato con il fosforo giallo e gli ossigeni rossi).
Esplorando la struttura
Il segnale portato da EGF può essere pericoloso
se usato in modo improprio. Molte forme di cancro ingannano il normale
processo di segnalazione EGF per avere il permesso di crescere senza
controllo. Per questo motivo i farmaci che bloccano la segnalazione
di EGF sono efficaci per il trattamento del cancro. Qui ne sono mostrati
tre esempi.
 Nella
figura qui a fianco si vede il farmaco lapatinib legato al dominio
chinasi del recettore (file PDB 1xkk).
Il farmaco blocca il processo di segnalazione all'interno della
cellula. Lapatinib è molto simile all'ATP, per questo si lega
fortemente nel sito attivo del recettore EGF al posto dell'ATP, il normale
legando. Nella
figura qui a fianco si vede il farmaco lapatinib legato al dominio
chinasi del recettore (file PDB 1xkk).
Il farmaco blocca il processo di segnalazione all'interno della
cellula. Lapatinib è molto simile all'ATP, per questo si lega
fortemente nel sito attivo del recettore EGF al posto dell'ATP, il normale
legando.
 Nel
trattamento del cancro vengono usati anche anticorpi. Nel
trattamento del cancro vengono usati anche anticorpi.
Nella figura qui a fianco si vede l'anticorpo erceptina (verde
e rosso) legato al dominio extracellulare di HER2/ErbB2 (file
PDB 1n8z).
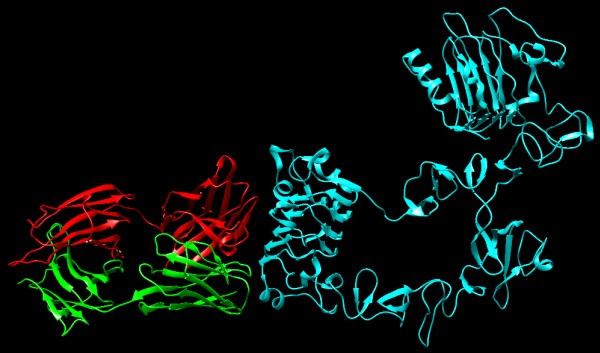 Infine
nell'immagine qui a fianco si vede l'anticorpo cetuximab (verde
e rosso) legato al dominio extracellulare del recettore EGF (file
PDB 1yy9). Il recettore, così legato,
non può dare dimeri e quindi non può indurre il segnale
di crescita all'interno della cellula. Infine
nell'immagine qui a fianco si vede l'anticorpo cetuximab (verde
e rosso) legato al dominio extracellulare del recettore EGF (file
PDB 1yy9). Il recettore, così legato,
non può dare dimeri e quindi non può indurre il segnale
di crescita all'interno della cellula.
Spunti per ulteriori esplorazioni
Compara il modo in cui dimerizza il recettore EGF e il recettore dell'ormone
della crescita.
Il recettore EGF e altri recettori simili sono attualmente dei bersagli
promettenti nello sviluppo di nuovi farmaci per la terapia del cancro.
Individua negli archivi PDB altri esempi di proteine legate a farmaci.
 Bibliografia Bibliografia
M. Lemmon (2009) Ligand-induced ErbB receptor dimerization.
Experimental Cell Research 315, 638-648.
R. Bose and X. Zhang (2009) The ErbB kinase domain: structural perspectives
into kinase activation and inhibition. Experimental Cell Research
315, 649-658.
K. M. Ferguson (2008) Structure-based view of epidermal growth factor
receptor regulation. Annual Review of Biophysics 37, 353-373.
|
|
|
 Introduzione
Introduzione
 Spegnere
il recettore
Spegnere
il recettore Nella
figura qui a fianco si vede il farmaco lapatinib legato al dominio
chinasi del recettore (file PDB
Nella
figura qui a fianco si vede il farmaco lapatinib legato al dominio
chinasi del recettore (file PDB 
 Infine
nell'immagine qui a fianco si vede l'anticorpo cetuximab (verde
e rosso) legato al dominio extracellulare del recettore EGF (file
PDB
Infine
nell'immagine qui a fianco si vede l'anticorpo cetuximab (verde
e rosso) legato al dominio extracellulare del recettore EGF (file
PDB