|
|
Ossidosqualene ciclasi |
|||||
|
Molecola del Mese di Dicembre 2007 L'enzima ossidosqualene ciclasi forma l'insolita struttura con quattro anelli fusi del colesterolo 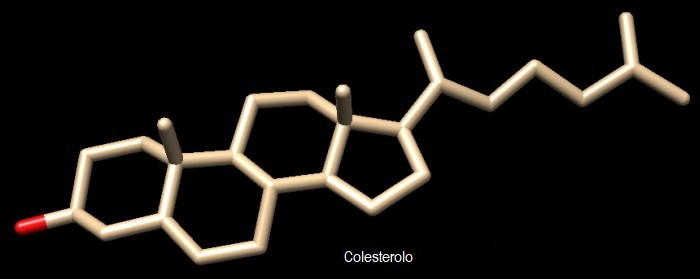 Introduzione IntroduzioneIl colesterolo, mostrato qui a fianco, è una grossa molecola lipidica composta di quattro anelli di atomi di carbonio fusi insieme e legati da una parte ad un gruppo OH, rosso, (da cui la desinenza olo) e dall'altra ad una catenella di 8 carboni. Il colesterolo si è guadagnato una pessima reputazione negli ultimi anni come una della cause di malattie cardiovascolari. Bisogna ricordare, però, che il colesterolo è essenziale per la nostra vita, infatti è indispensabile per mantenere fluide le membrane cellulari e inoltre costituisce il materiale di partenza per sintetizzare molte molecole importanti come la vitamina D e gli ormoni steroidei. D'altra parte, però, elevati livelli di colesterolo, prodotti per esempio da una dieta ricca di grassi, possono causare l'insorgere di malattie cardiovascolari come l'aterosclerosi che a sua volta può portare all'ictus o all'infarto. I medici suggeriscono che una dieta povera di grassi e un po' di esercizio fisico svolto quotidianamente possono prevenire questi effetti negativi del colesterolo. 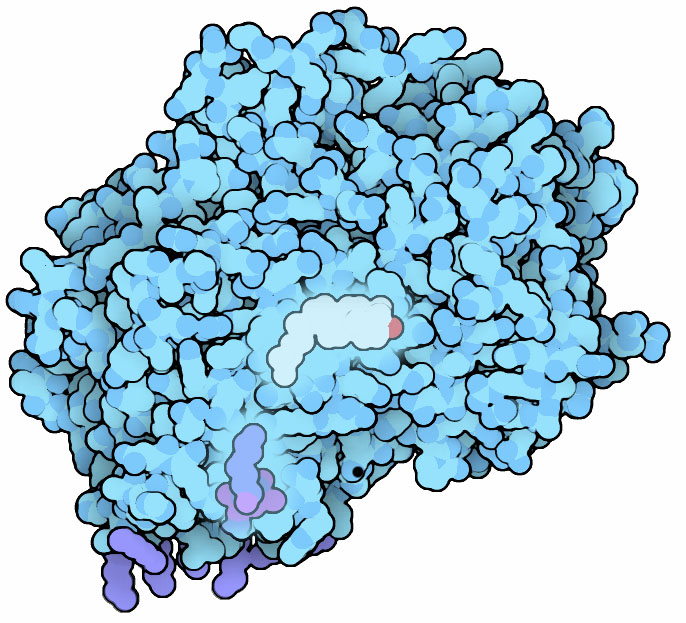 Sintetizzare
colesterolo Sintetizzare
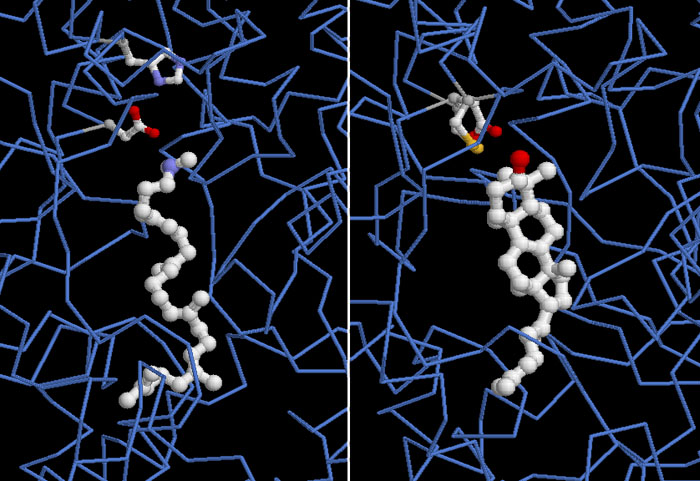
colesteroloUn insieme di una ventina di enzimi è coinvolto nella sintesi del colesterolo a partire da molecole iniziali molto semplici. L'enzima mostrato qui a fianco, ossidosqua-lene ciclasi (file PDB 1w6k), realizza il passaggio più complicato di tutto il processo. Prende una lunga catena idrocarburica, l'ossidosqualene, la ripiega e realizza i quattro anelli. La struttura dell'enzima mostrata qui ha ancora legato nel sito attivo il prodotto della reazione enzimatica, il lanosterolo, evidenziato nel centro con un colore più chiaro e mostrato anche più sotto. Substrati grassi Sia l'ossidosqualene che il colesterolo sono essenzialmente degli idrocarburi e quindi sono praticamente insolubili in acqua, mentre sono solubili nei grassi ed in particolare sono solubili all'interno della membrana cellulare che è formata di fosfolipidi. L'enzima risolve questo problema di solubilità legandosi alla membrana all'interno della cellula così può estrarre l'ossidosqualene direttamente dalla membrana e poi può rilasciare nella membrana il lanosterolo prodotto. Nella figura qui a destra si possono vedere alcuni di questi lipidi (viola) che, provenendo dalla membrana (in basso), si affacciano verso l'enzima. Uno di questi lipidi si sta infilando nel tunnel che porta nel sito attivo all'interno dell'enzima. . . . . . . . . . . . . . . . 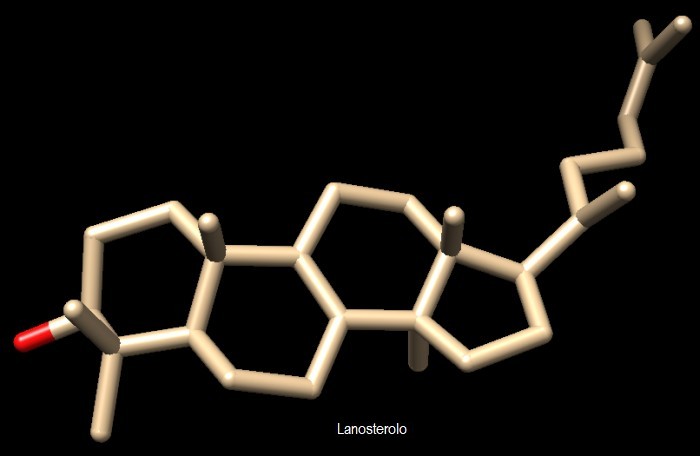 Abbassare i livelli di colesterolo 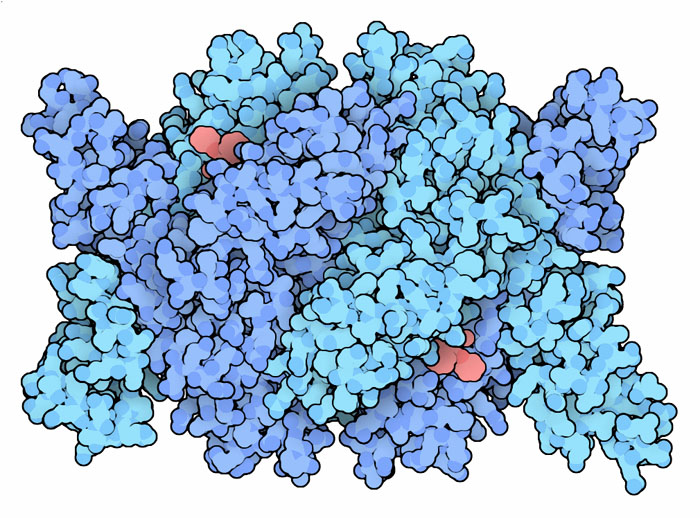 I
farmaci che riducono i livelli di colesterolo nel sangue sono tra i più
venduti nel mondo. Quelli prescritti più frequentemente sono le
statine che bloccano l'azione di un enzima che realizza uno dei
primi passaggi nella sintesi del colesterolo. L'enzima HMG-CoA reduttasi
(file PDB 1hwk) è illustrato qui
a fianco con il farmaco atorvastatina (rosso) legato nel suo sito
attivo. I
farmaci che riducono i livelli di colesterolo nel sangue sono tra i più
venduti nel mondo. Quelli prescritti più frequentemente sono le
statine che bloccano l'azione di un enzima che realizza uno dei
primi passaggi nella sintesi del colesterolo. L'enzima HMG-CoA reduttasi
(file PDB 1hwk) è illustrato qui
a fianco con il farmaco atorvastatina (rosso) legato nel suo sito
attivo. L'atorvastatina è illustrata anche qui sotto in una immagine realizzata con Chimera. I ricercatori stanno ora cercando nuovi farmaci capaci di bloccare altri passaggi della sintesi del colesterolo come, per esempio, la reazione catalizzata dall'enzima ossidosqualene ciclasi. . . . . . . . . . . . . . . . . . 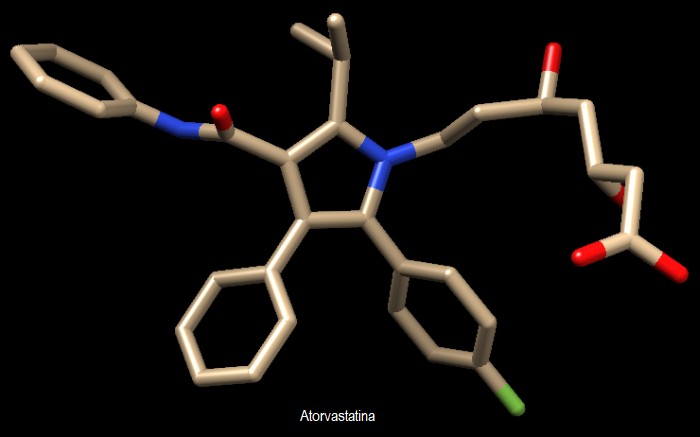
|
||||||
|
|
||||||