|
|
Serpina |
|||||
|
Molecola del mese di maggio 2004 Le serpine sono enzimi-trappola che catturano e avviano alla distruzione le proteasi pericolose 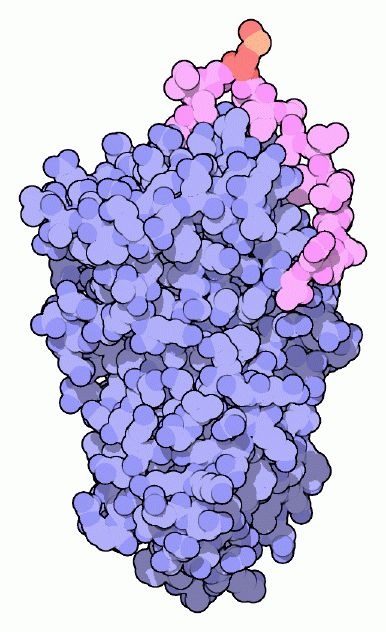 Introduzione IntroduzioneLe nostre cellule spesso devono utilizzare strumenti pericolosi come gli enzimi che servono per demolire le grandi molecole. Tra questi ricordiamo gli enzimi chiamati nucleasi che rompono il DNA e l'RNA, le amilasi che rompono i carboidrati, le lipasi che spezzano i lipidi, e le proteasi che smontano le proteine. Questi enzimi distruttivi sono necessari in molte situazioni. Vengono usati nella digestione, per rompere le macromolecole del cibo in frammenti utilizzabili. Sono usati nella difesa, per attaccare i virus e i batteri invasori. Sono usati per rompere le molecole difettose o inutili nelle cellule. Vengono usati anche nelle segnalazioni, per attivare immediatamente le molecole di segnalazione quando giunge un messaggio. Questi enzimi sono essenziali quando sono usati nel posto giusto e al momento giusto, ma possono provocare disastri se vanno fuori controllo. Protezione dalle proteasi Per controllare queste macchine distruttive, le nostre cellule costruiscono un insieme di proteine per bloccare la loro azione e neutralizzare il pericolo. Le serpine sono una classe di queste molecole, progettate per cercare e distruggere alcune specifiche proteasi alla serina. Il nome serpina, anche se ricorda un serpente, deriva dalla loro funzione: inibitori delle proteasi alla serina (serine protease inhibitor). L'esempio mostrato qui a destra è la alfa-1-antitripsina, dall'archivio PDB 1psi. Si trova nel sangue, dove protegge i tessuti circostanti dalla elastasi, un enzima che taglia le proteine. I linfociti neutrofili (un tipo di globuli bianchi) secernono la elastasi nei siti di infiammazione, questa rompe il tessuto connettivo e permette alle cellule del sangue di entrare per svolgere il loro compito di difesa e riparazione.(Per questo il tessuto infiammato è gonfio, arrossato e dolente). La serpina protegge le aree vicine ed assicura che l'elastasi non si diffonda in tutto il corpo. Intrappolare le proteasi La serpina è una macchina molecolare che funziona in modo simile ad una trappola per topi, completa di esca e braccio a molla. E' una proteina metastable, cioè è solo parzialmente stabile nella sua forma attiva e, quando trova una proteasi, può scattare per assumere una forma molto più stabile. La chiave di questo movimento è un tratto di catena flessibile, mostrato qui in rosa. Un amminoacido in questo tratto è usato come esca. Nella alpha-1-antitripsina, è una metionina, mostrata qui in rosso e arancione. Come è descritto nelle prossime due pagine, le proteasi vengono catturate e distrutte quando attaccano questa esca. Un nido di serpine Sono state studiate più di trenta serpine umane diverse (alcune di queste sono disponibili negli archivi PDB), ognuna ha un compito essenziale e diverso. Molte si trovano nel sangue. Alcune controllano il processo della coagulazione del sangue: la antitrombina limita l'azione della trombina quando si forma il coagulo, e la antiplasmina limita l'azione della plasmina quando i coaguli di sangue vengono degradati. Altre serpine controllano l'azione delle proteasi usate nel sistema complementare che ci protegge dalle infezioni batteriche. Quando le serpine falliscono Quando le serpine falliscono, si possono produrre gravi danni. Due sono i problemi più frequenti. Una serpina può essere difettosa, così non è capace di bloccare il suo bersaglio molecolare e lascia le proteasi libere di compiere devastazioni. Questo avviene, per esempio, nell'enfisema polmonare, quando una alfa-1-antitripsina difettosa permette alla elastasi di distruggere il tessuto connettivo dei polmoni. Una delle cause della inattivazione delle serpine è il fumo di sigaretta che può modificare la metionina, l'amminoacido usato come esca. In alternativa, il meccanismo unico di trappola delle serpine, mostrato in maggior dettaglio qui sotto, può condurre ad un altro problema. Dopo che il tratto di catena viene rotto, si può associare con altre molecole di serpina, producendo grossi aggregati. Se questi si formano all'interno delle cellule nervose, si blocca la funzione nervosa di intere aree del cervello e questo può condurre alla demenza. 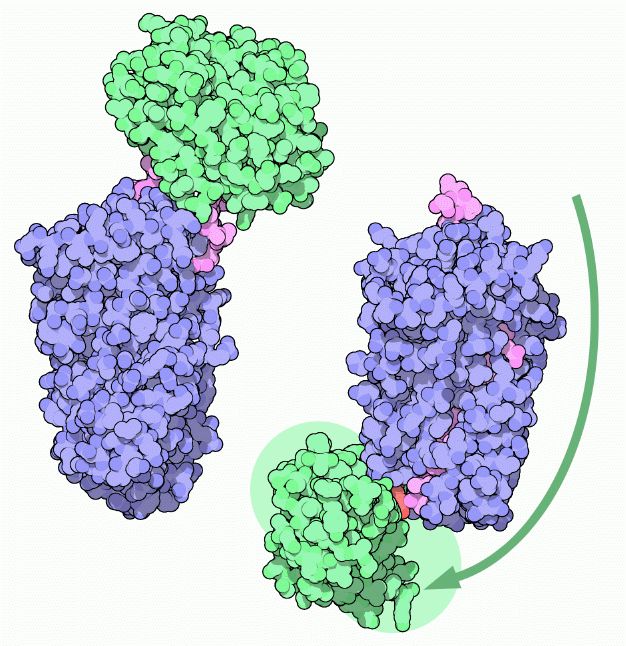 Far
scattare la trappola Far
scattare la trappola Il filamento flessibile delle serpine, noto come il filamento del centro reattivo, è l'esca e il braccio a molla della trappola. La proteasi, mostrata qui in verde, si lega all'esca (rosa) e comincia a compiere la sua normale reazione di taglio della catena proteica. La struttura sulla sinistra (file PDB 1k9o) mostra la tripsina (verde) subito dopo che si è legata. La serina reattiva della proteasi attacca il filamento, forma un legame estere con la catena, e realizza il taglio. Normalmente a questo punto dovrebbe intervenire una molecola di acqua, per liberare la proteasi dalla sua molecola bersaglio. Ma invece la serpina (blu) prende il controllo prima che la sfortunata tripsina possa liberarsi. Il filamento flessibile, appena tagliato, è libero di muoversi e scatta portandosi all'interno di una vasta fenditura sul lato della serpina, trascinando con sè la proteasi (verde) dall'altro lato della serpina, come mostrato nella struttura qui sopra a destra (file PDB 1ezx). Si potrebbe pensare che la tripsina potesse ancora compiere il resto della sua reazione e liberarsi. Ma il filamento della serpina, bloccato fermamente nella fenditura, è troppo corto, così la tripsina resta bloccata e in tensione contro il fondo della serpina. Questo deforma il sito attivo della tripsina, tanto da renderlo inattivo. La tripsina deformata perde in parte il suo corretto ripiegamento. Questo la trasforma in un facile bersaglio per l'apparato cellulare che spazza via le proteine difettose e così distrugge sia la proteasi che la serpina, un enzima che quindi può agire una sola volta. Esplorando la struttura Le due straordinarie strutture cristallografiche illustrate qui sotto ci mostrano la situazione iniziale e finale dell'azione della alfa-1-antitripsina. Qui sotto (file PDB 1k9o) vediamo il complesso serpina-proteasi prima che scatti la trappola. Gli scienziati hanno usato una forma mutante della proteasi, con la serina reattiva sostituita da una alanina (Ala, rosa), per poter osservare il complesso senza fare scattare la trappola. La tripsina (ciano) ha catturato un filamento della serpina (magenta) e lo ha legato in corrispondenza di un amminoacido basico, lisina (Lys, beige), ma non è in grado di tagliarlo con l'amminoacido mutante alanina. Notate le quattro lunghe catene parallele nella serpina (gialle). 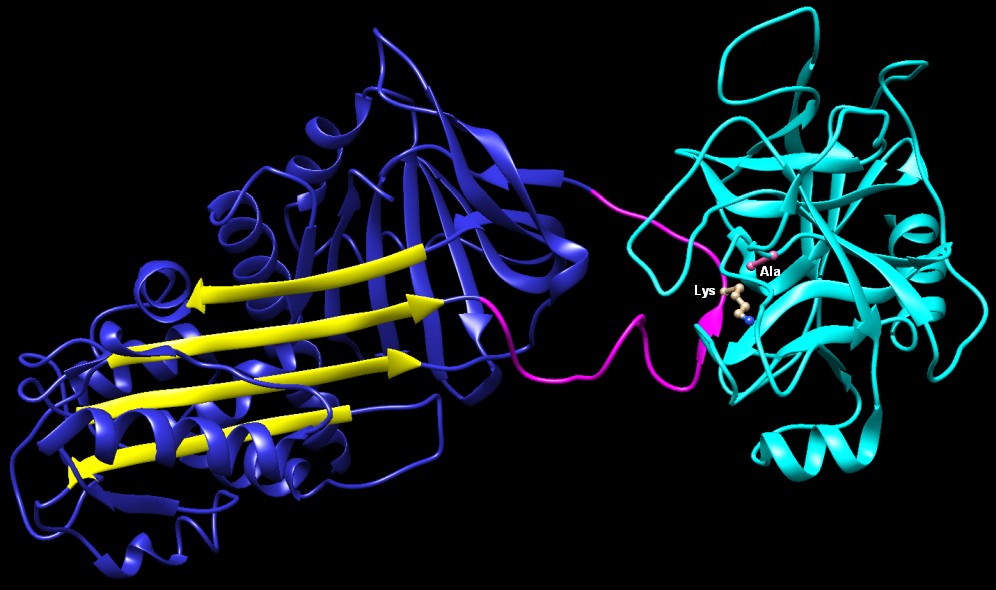 Qui sotto (file PDB 1ezx) vediamo il complesso dopo che è scattata la trappola: il filamento magenta è stato tagliato, e la tripsina (verde) è stata trascinata dall'altro lato della serpina. La serina reattiva (Ser, rosa) della tripsina è unita con legame covalente alla metionina (Met, beige) della serpina dove è avvenuto il taglio della proteasi. Notate che la catena del filamento tagliato (magenta) è scattata portandosi in mezzo alle quattro catene parallele (gialle). Notate anche che la tripsina si è deformata e il suo sito attivo non è più in grado di rompere il legame estere che aggancia la serina della proteasi al filamento tagliato (magenta) della serpina. Gran parte della catena proteica non è visibile nella struttura cristallina perché non aveva una posizione definita nel cristallo. I tratteggi mostrano i punti dove la struttura sperimentale finisce e i filamenti non sono più visibili. 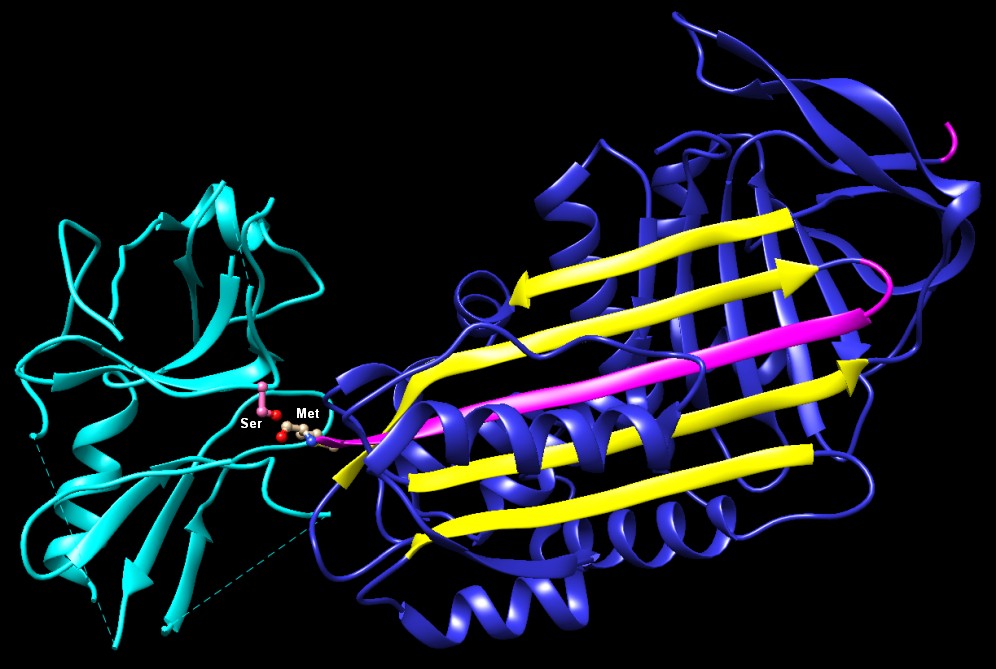
P. G. W. Gettins (2002) Serpin structure, mechanism and function. Chemical Reviews 102, 4751-4803. R. N. Pike and others (2002) Serpins: Finely balanced conformational traps. IUBMB Life 54, 1-7 G. A. Silverman and others (2001) The serpins are an expanding superfamily of structurally similar but functionally diverse proteins. Journal of Biological Chemistry 276, 33293-33296. J. Protempa, E. Korzus and J. Travis (1994) The serpin superfamily of proteinase inhibitors: Structure, function and regulation. Journal of Biological Chemistry 269, 15957-15960.
|
||||||
|
|
||||||
