|
Molecola del mese di maggio 2001
Il bersaglio dell'aspirina è la
cicloossigenasi che sintetizza le prostaglandine dell'infiammazione e
della coagulazione del sangue
 Aspirina Aspirina
Quale è il farmaco più diffuso oggi? È un efficace
analgesico. Riduce la febbre e l'infiammazione quando il corpo diventa
troppo zelante nel difendersi contro le infezioni e le contusioni. Rallenta
la coagulazione del sangue, riducendo la probabilità di ictus e
di attacco cardiaco nelle persone predisposte. Inoltre, ci sono sempre
più evidenze che sia un efficace aiuto anche nella lotta contro
il cancro. Questo farmaco incredibile, e dalle applicazioni così
varie, è l'aspirina.
L'aspirina viene usata professionalmente da circa un secolo, ma è
stata usata in modo empirico fin dall'antichità. Un composto simile
che si trova nella corteccia del salice, l'acido salicilico, viene utilizzato
da molto tempo in erboristeria. Ma solo negli ultimi decenni abbiamo capito
il meccanismo d'azione dell'aspirina, e come si potrebbe migliorarlo.
 Prostaglandine Prostaglandine
Come è logico aspettarsi da un farmaco con azioni così diverse,
l'aspirina blocca un processo fondamentale nel corpo, la produzione delle
prostaglandine, importanti ormoni che vengono usati per trasportare messaggi
a livello locale. Contrariamente alla maggior parte degli ormoni, che
sono prodotti in ghiandole specializzate e poi trasportati in tutto il
corpo dal sangue, le prostaglandine vengono sintetizzate localmente dalle
cellule e poi agiscono solo nell'area circostante prima di essere demolite.
Le prostaglandine controllano molti processi locali come la secrezione
di acido nello stomaco, la contrazione delle cellule muscolari attorno
ai vasi sanguigni, l'aggregazione delle piastrine durante la coagulazione
del sangue, la contrazione uterina durante il travaglio. Le prostaglandine
inoltre trasmettono e rinforzano i segnali del dolore e provocano vasodilatazione
e quindi infiammazione. Questi processi così diversi sono controllati
da prostaglandine diverse, che però vengono tutte sintetizzate
a partire da una sola molecola capostipite, l'acido arachidonico.
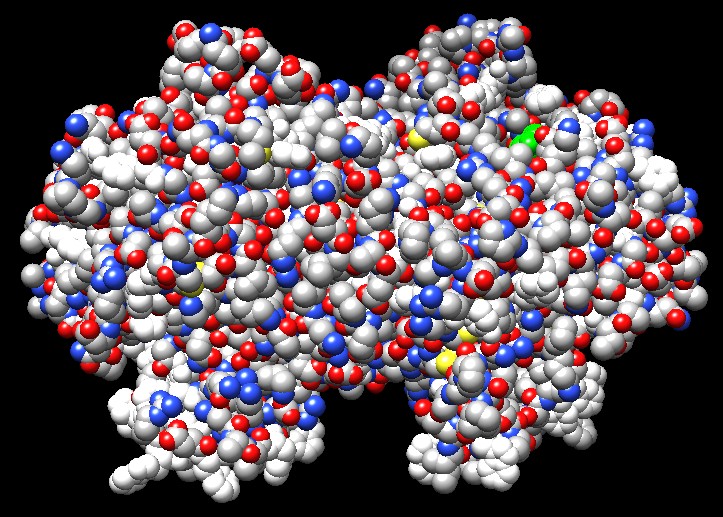
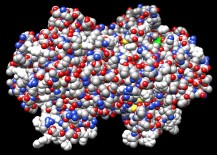
La cicloossigenasi (mostrata qui sopra, file PDB 3n8w)
compie il primo passo nella sintesi delle prostaglandine a partire da
un comune acido grasso, l'acido arachidonico. Usando un gruppo
eme simile a quello dell'emoglobina (visibile in verde nella figura),
fissa molecole di ossigeno O2 e le fa reagire
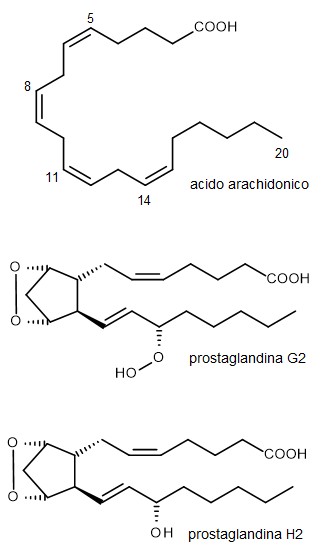
con l'acido arachidonico. Come è illustrato nel riquadro qui a
destra, aggiunge due molecole di ossigeno all'acido arachidonico e forma
un anello a cinque atomi, formando dapprima la prostaglandina G2 nella
quale vi sono due legami perossido (O-O), poi rompe uno di questi legami
con la sua attività di perossidasi formando la prostaglandina H2.
Questa, attraverso altri enzimi, viene poi convertita in una varietà
di prostaglandine diverse.
L'aspirina impedisce il legame dell'acido arachidonico nel sito
attivo della cicloossigenasi impedendo così la sintesi della prostaglandina
H2 e delle altre prostaglandine da questa derivate e così non sentiamo
il dolore e non inneschiamo la risposta infiammatoria.
COX-1 e COX-2
In realtà noi possediamo due cicloossigenasi diverse (chiamate
COX-1 e COX-2) e le utilizziamo per scopi diversi. La COX-1 è
presente in quasi tutte le nostre cellule, sintetizza le prostaglandine
usate in tutto il corpo per mantenere una corretta fisiologia. Il secondo
enzima, la COX-2, viene prodotto solo occasionalmente e solo nelle cellule
coinvolte nella risposta infiammatoria o immunitaria. Causa dolore e
gonfiore in risposta ad un danno fisico o ad un infezione, aumenta la
permeabilità delle pareti dei vasi sanguigni e fa giungere le
cellule del sistema immunitario al tessuto danneggiato.
Sfortunatamente, l'aspirina attacca entrambe le cicloossigenasi.
Dato che colpisce anche la COX-1, l'aspirina può condurre a complicazioni
sgradevoli, come l'emorragia gastrica. Fortunatamente, stanno diventando
disponibili farmaci specifici in grado di bloccare prevalentemente la
COX-2, lasciando libera la COX-1 di svolgere i suoi compiti essenziali.
Queste nuovi farmaci sono antidolorifici e antipiretici selettivi, e
producono solo in minima parte gli effetti collaterali indesiderati
tipici dell'aspirina.
 Un
enzima complesso Un
enzima complesso
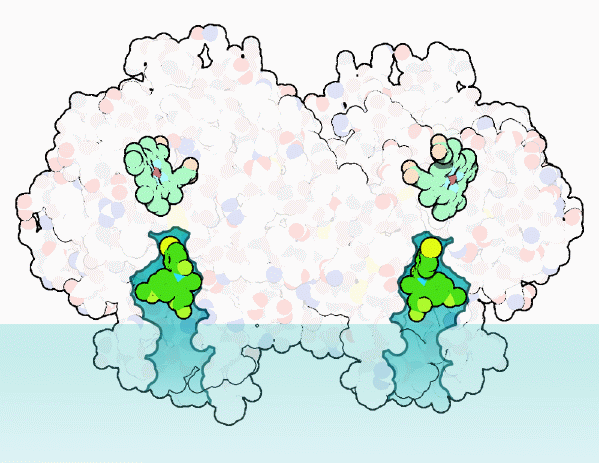
Questo enzima, in realtà, ha due siti attivi diversi, chiamati
complessivamente prostaglandina sintasi. Al centro c'è il sito
attivo di cicloossigenasi, più in alto c'è il sito di
perossidasi completamente separato dall'altro, necessario per attivare
i gruppi eme che partecipano alla reazione di cicloossigenasi. Il complesso
enzimatico in realtà è un dimero composto di due subunità
identiche affiancate, così ci sono due siti attivi di cicloossigenasi
e due siti attivi di perossidasi molto vicini gli uni agli altri. Inoltre,
ogni subunità, in basso, ha una piccola protuberanza ricca di
catene idrocarburiche apolari (bianche) ben visibile anche nella figura
in alto nella pagina. Queste protuberanze ancorano il complesso alla
membrana del reticolo endoplasmatico, rappresentata qui a lato in azzurro.
Il sito attivo di cicloossigenasi è nascosto in profondità
all'interno della proteina, ed è raggiungibile attraverso un
tunnel che sbuca al centro della protuberanza. Il tunnel si comporta
come un imbuto, guidando l'acido arachidonico sciolto nella membrana
fino all'interno dell'enzima dove viene fatto reagire. Nella struttura
mostrata qui a fianco (file PDB 4cox),
un farmaco (giallo e verde, indometacina) sta bloccando il sito attivo
in entrambe le subunità. In ogni subunità sono anche visibili
i gruppi eme sopra le molecole del farmaco.
Esplorando la struttura
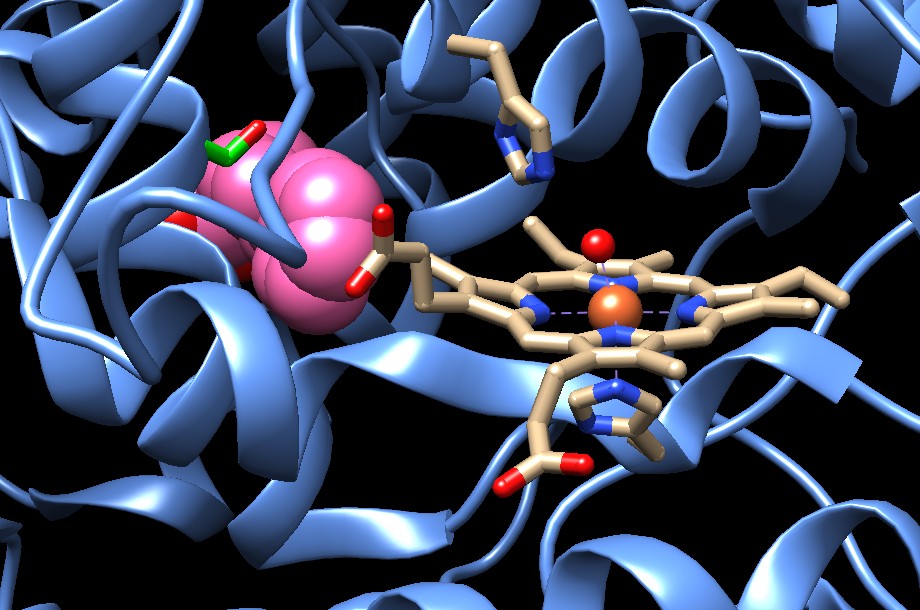
La figura qui sotto mostra una COX-1 (file PDB 3n8w)
che sta legando un farmaco antiinfiammatorio (flurbiprofene, rosa).
Il farmaco è entrato nel sito attivo al posto dell'acido arachidonico
e si è portato vicino al gruppo eme in primo piano. L'eme è
tenuto in posizione da due istidine, una sotto (più vicina) ed
una sopra. A centro dell'eme, l'atomo di ferro (arancione) lega una
molecola d'acqua, di cui si vede solo l'ossigeno rosso, in quello stesso
punto il ferro può legare l'ossigeno O2.
Sulla sinistra si vede la serina 530 (verde) che si trova appena sopra
il farmaco. Il sito attivo non è stato modificato dal flurbiprofene,
così, quando il farmaco abbandona il sito attivo, la COX-1 può
tornare a compiere la sua reazione sull'acido arachidonico producendo
ancora prostaglandine.
. . . . 
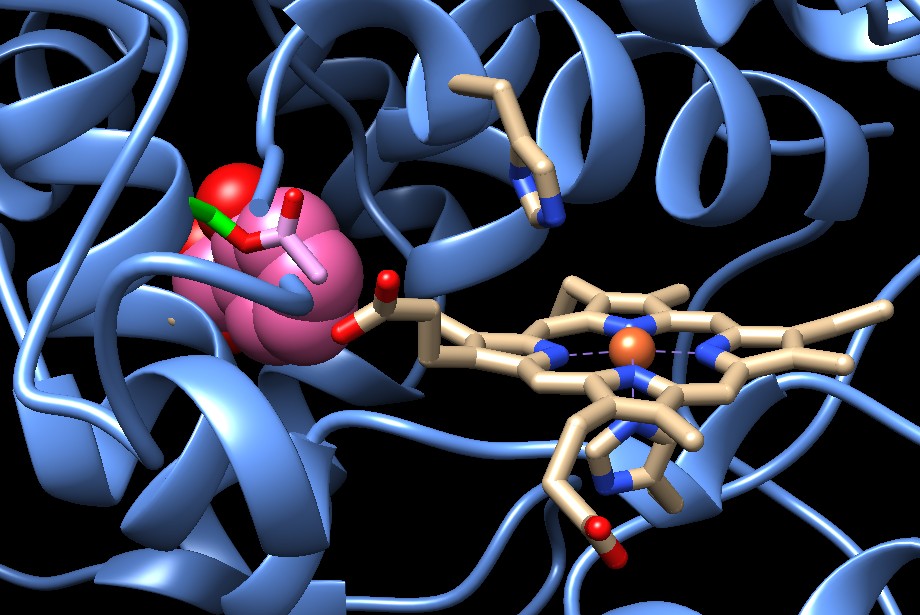
La prossima figura mostra come l'aspirina blocca in modo permanente
il sito attivo della cicloossigenasi. L'aspirina è composta da
una molecola di acido salicilico legata ad un gruppo acetilico. Quando
l'aspirina attacca la cicloossigenasi, trasferisce il suo gruppo acetilico
ad un amminoacido di serina (Ser 530), disattivando irreversibilmente
l'enzima. La figura qui sotto mostra un primo piano del sito attivo
di una COX-1 (file PDB 1pth) dopo che
l'aspirina ha compiuto la sua opera. Il gruppo acetilico (rosa chiaro)
è legato all'amminoacido serina (verde), e l'acido salicilico
(sfere rosa) è legato subito dietro. Il sito attivo è
stato modificato in modo permanente, così, quando il farmaco
abbandona il sito attivo, la COX-1 resta disattivata e non può
più compiere la sua reazione sull'acido arachidonico. Le prostaglandine
potranno ancora essere sintetizzate solo quando la cellula produrrà
nuove cicloossigenasi.
. . . . 
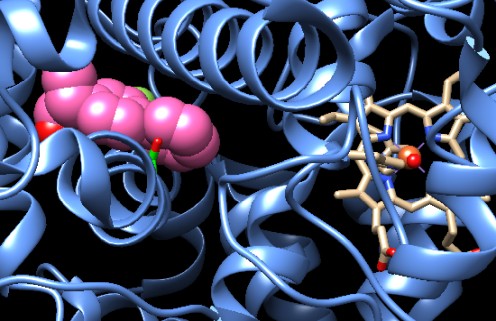
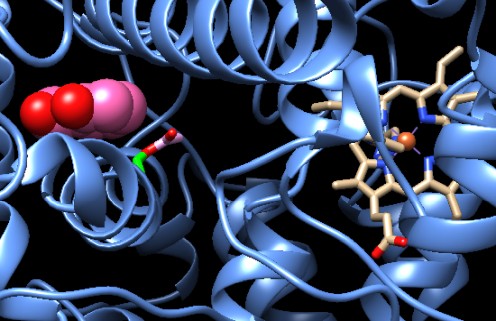
Nella prossima figura il sito attivo è mostrato
dall'alto in modo da apprezzare come la serina acetilata blocchi l'accesso
alla parte più profonda del sito attivo.
Dato che l'aspirina disattiva in modo permanente le cicloossigenasi,
nella terapia anticoagulante per prevenire le ricadute dell'infarto,
viene prescritta l'aspirinetta 100 mg che contiene una quantità
di acido acetilsalicilico 5 volte inferiore all'aspirina. Ne basta una
compressa ogni 24 ore, mentre altri farmaci antiinfiammatori hanno un'azione
che dura solo poche ore.
 Bibliografia Bibliografia
Lawrence J. Marnett, Scott W. Rowlinson, Douglas C. Goodwin, Amit S.
Kalgutkar and Cheryl A. Lanzo (1999) Arachidonic Acid Oxygenation by
COX-1 and COX-2. Journal of Biological Chemistry 274,
22903-22906.
William L. Smith, R. Michael Garavito and David L. DeWitt (1996) Prostaglandin
Endoperoxide H Synthases (Cyclooxygenases)-1 and -2. Journal of Biological
Chemistry 271, 33157-33160.
|
|
|
 Aspirina
Aspirina
 Prostaglandine
Prostaglandine

 Un
enzima complesso
Un
enzima complesso


