Pianeta
Chimica.it
Responsabile:
Prof. Mauro Tonellato
Guida alla interpretazione
degli spettri
NMR 1H
Per interpretare uno spettro NMR, è opportuno seguire la
seguente procedura:
1) Contate il numero di picchi nello
spettro. Corrispondono agli idrogeni chimicamente diversi nella molecola
incognita.
2) Sommate l’area di ogni picco e confrontatela con
il numero di idrogeni presenti nella formula bruta per capire a quanti
idrogeni corrisponde ogni picco.
3) Analizzare la formula bruta e gli altri dati disponibili
per individuare i gruppi funzionali e la eventuale presenza di doppi legami
o di anelli.
4) Analizzate i chemical shift di ogni picco per capire
che tipo di idrogeni sono presenti nella molecola. Usate le tabelle A
e B per aiutarvi nella interpretazione.
5) Analizzate la molteplicità m di ogni picco per
capire quanti idrogeni sono vicini all’idrogeno in questione applicando
la formula: H vicini = m – 1.
6) Cominciate ad analizzare lo spettro da sinistra, cioè
dagli idrogeni più deschermati, quelli legati ai gruppi funzionali.
7) Scrivete la struttura di ogni piccola porzione di molecola individuata,
cominciando dal gruppo funzionale e individuando le sequenze di atomi
concatenati sfruttando gli accoppiamenti di spin tra idrogeni vicini.
8) Utilizzate i dati raccolti per ipotizzare una struttura molecolare.
9) Verificate che la formula bruta, i chemical shift, le aree dei
picchi e le molteplicità per la molecola proposta siano compatibili
con i dati dello spettro incognito.
(Usate le tabelle A e B per aiutarvi nella interpretazione degli spettri NMR)
![]()
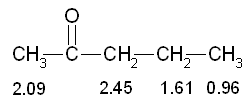
Usiamo questa procedura per interpretare il seguente spettro NMR. E’ lo spettro di una molecola di formula bruta C5H10O che possiede un carbonile come si deduce dal suo spettro IR (non mostrato).

1) Nello spettro NMR sono presenti
4 picchi distinti, quindi sappiamo che nella molecola ci sono quattro
tipi di idrogeni diversi.
2) L’area dei picchi dà come somma 10 quindi l’area
dichiarata in cima ai picchi corrisponde al numero di idrogeni che producono
quel segnale.
3) Dall'analisi della formula bruta C5H10O
osserviamo che, se la molecola fosse satura, dovrebbe avere (2n+2) idrogeni
cioè 5+5+2 = 12 idrogeni. Dato che ne ha 10, mancano 2 idrogeni,
1 coppia, quindi la molecola ha una insaturazione. Poichè è
presente un carbonile, l’insaturazione è il doppio legame
del carbonile, il resto della molecola è saturo.
4) Dato che la molecola contiene un carbonile, i
due segnali a 2,45 e 2,09 ppm corrispondono agli idrogeni di un
CH2 e di un CH3 vicini
al carbonile che assorbono nell'intervallo tra 2 e 3 ppm. Gli altri due
picchi a 1.61 e 0,96 ppm corrispondono invece ad un CH2
e ad un CH3 più lontani dal carbonile.
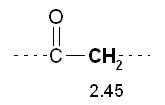 5)
Cominciamo ad analizzare lo spettro da sinistra. Il primo segnale è
il tripletto di area 2 a 2.45 ppm. E dovuto ad un CH2
legato al carbonile. Infatti un CH2 in quella
posizione, secondo i dati in tabella B, dovrebbe assorbire intorno a 2.3
ppm (1.3 CH2 + 1.0 CO = 2.3 ppm), un valore
vicino ai 2.45 ppm osservati.
5)
Cominciamo ad analizzare lo spettro da sinistra. Il primo segnale è
il tripletto di area 2 a 2.45 ppm. E dovuto ad un CH2
legato al carbonile. Infatti un CH2 in quella
posizione, secondo i dati in tabella B, dovrebbe assorbire intorno a 2.3
ppm (1.3 CH2 + 1.0 CO = 2.3 ppm), un valore
vicino ai 2.45 ppm osservati.
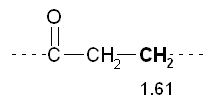 6)
Dato che il CH2 a 2.45 ppm è un tripletto,
deve avere 2 idrogeni vicini, quindi è legato ad un altro CH2.
L’unico possibile è il CH2 sestetto
a 1.61 ppm.
6)
Dato che il CH2 a 2.45 ppm è un tripletto,
deve avere 2 idrogeni vicini, quindi è legato ad un altro CH2.
L’unico possibile è il CH2 sestetto
a 1.61 ppm.
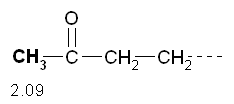 7)
Il secondo segnale nello spettro è il singoletto di area
3 a 2.09 ppm. E’ dovuto ad un CH3
legato al carbonile, questo, infatti, per i dati in tabella B, dovrebbe
assorbire intorno a 1.9 ppm (0.9 CH3 + 1.0 CO
= 1.9 ppm), un valore vicino ai 2.09 ppm osservati. Il fatto che sia singoletto
ci conferma che non ha idrogeni vicini, in accordo con la struttura che
abbiamo ipotizzato qui a destra.
7)
Il secondo segnale nello spettro è il singoletto di area
3 a 2.09 ppm. E’ dovuto ad un CH3
legato al carbonile, questo, infatti, per i dati in tabella B, dovrebbe
assorbire intorno a 1.9 ppm (0.9 CH3 + 1.0 CO
= 1.9 ppm), un valore vicino ai 2.09 ppm osservati. Il fatto che sia singoletto
ci conferma che non ha idrogeni vicini, in accordo con la struttura che
abbiamo ipotizzato qui a destra.
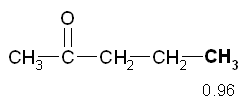 8)
L’ultimo segnale nello spettro è il tripletto di area
3 a 0.96 ppm. E’ dovuto ad un semplice CH3
lontano dai gruppi funzionali, che, infatti, dovrebbe assorbire a 0.9
ppm, secondo i dati in tabella B. Dato che è un tripletto, ha due
idrogeni vicini, quindi è legato al CH2
a 1.61 ppm.
8)
L’ultimo segnale nello spettro è il tripletto di area
3 a 0.96 ppm. E’ dovuto ad un semplice CH3
lontano dai gruppi funzionali, che, infatti, dovrebbe assorbire a 0.9
ppm, secondo i dati in tabella B. Dato che è un tripletto, ha due
idrogeni vicini, quindi è legato al CH2
a 1.61 ppm.
9) Per confermare la struttura trovata fin qui, verifichiamo che anche
la molteplicità del CH2 a 1.61 ppm sia
giustificata. Questo è un sestetto, quindi ha 5 idrogeni vicini.
Nella struttura proposta vediamo che è legato ad un CH2
a sinistra e un CH3 a destra, quindi ha vicini
proprio 5 idrogeni.
Questo ci permette di confermare la correttezza della molecola trovata.
Si tratta di pentan-2-one
2-pentanone
![]()
Questa Guida è disponibile anche in formato PDF per poterla stampare con maggior facilità